
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Уравнение политропного процесса
|
|
Энтропия идеальных газов
Для получения рассчетного выражения изменения энтропии идеальных газов воспользуемся первым законом термодинамики, в котором теплота определяется с использованием изменения энтальпии

| (4.58) |
Для идеального газа изменение энтальпии определяется как dh=cPdT, а удельный объем v=RT/P. Подставив данные выражения изменения энталпии и удельного объема в уравнение (4.58), получим уравнение для изменения энтропии идеального газа

| (4.59) |
Разность энтропий идеального газа в конкретных двух состояниях можно получить интегрированием выражения (4.59)

| (4.60) |
Воспользовавшись формулой Майера сР=сV+R и уравнением Менделеева-Клапейрона Pv=RT, выражение (4.60) можно записать и через две другие пары термических параметров состояния

| (4.61) |
Для определения абсолюного значения энтропии идеального газа необходимо зафиксировать начало ее отсчета любой парой термических параметров состояния. Например, приняв s0=0 при Т0 и Р0, воспользовавшись уравнением (4.60), получим

| (4.62) |
Выражение (4.62) свидетельствует о том, что энтропия идеального газа есть параметр состояния, поскольку ее можно определить через любую пару параметров состояния. В свою очередь, поскольку энтропия сама является параметром состояния, используя ее в паре с любым независимым параметром состояния, можно определить любой другой параметр состояния газа.
68 Тепловыми маши́нами КПД
Тепловыми маши́нами в термодинамике называются тепловые двигатели и холодильные машины (термокомпрессоры)[1]. Разновидностью холодильных машин являются тепловые насосы.
Тепловые двигатели осуществляют превращение тепла в работу. Для функционирования тепловой машины необходимы следующие составляющие: нагреватель, холодильник и рабочее тело. При этом тепло к рабочему телу подводится от нагревателя, имеющего более высокую температуру  , и частично отводится к холодильнику, имеющего более низкую температуру
, и частично отводится к холодильнику, имеющего более низкую температуру  . Необходимость наличия нагревателя и рабочего тела обычно не вызывает сомнений, что же касается холодильника, как конструктивной части тепловой машины, то он может отсутствовать. В этом случае его функцию выполняет окружающая среда.
. Необходимость наличия нагревателя и рабочего тела обычно не вызывает сомнений, что же касается холодильника, как конструктивной части тепловой машины, то он может отсутствовать. В этом случае его функцию выполняет окружающая среда.
Работа, произведённая тепловым двигателем, согласно первому началу термодинамики равна разности количеств тепла подведённого  и отведённого
и отведённого  :
:
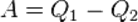
Коэффициентом полезного действия (КПД) теплового двигателя называется отношение произведённой работы к подведённому извне количеству тепла:

Холодильные машины осуществляют процесс переноса тепла от источников с более низким температурным уровнем  к источникам более высоким температурным уровнем
к источникам более высоким температурным уровнем  . Для осуществления этого процесса, называемого термокомпрессией, затрачивается подводимая внешняя работа:
. Для осуществления этого процесса, называемого термокомпрессией, затрачивается подводимая внешняя работа:
 .
.
Эффективность работы холодильных машин определяется величиной удельной холодопроизводительности, представляющей отношение отнятой от охлаждаемого тела теплоты к затраченной для этого механической работе :

Холодильная машина может быть использована не только для охлаждения различных тел, но и для отопления помещений. Действительно, даже обычный бытовой холодильник, охлаждая помещённые в нём продукты, одновременно нагревает воздух в комнате. Принцип действия, лежащий в основе современных тепловых насосов, заключается в использовании обращённого цикла тепловой машины для перекачки теплоты из окружающей среды в помещение. Основное отличие теплового насоса от холодильной машины состоит в том, что теплота  подводится к нагреваемому телу, например, к воздуху обогреваемого помещения, а теплота
подводится к нагреваемому телу, например, к воздуху обогреваемого помещения, а теплота  отнимается от менее нагретой окружающей среды. Эффективность теплового насоса характеризуется коэффициентом преобразования (трансформации) или, как часто называют, отопительным коэффициентом
отнимается от менее нагретой окружающей среды. Эффективность теплового насоса характеризуется коэффициентом преобразования (трансформации) или, как часто называют, отопительным коэффициентом  , который определяется как отношение полученной нагреваемым телом теплоты
, который определяется как отношение полученной нагреваемым телом теплоты  к затраченной для этого механической работе, либо работе электрического тока
к затраченной для этого механической работе, либо работе электрического тока  :
: 
Учитывая, что  , устанавливаем связь между отопительным и холодильным коэффициентами установки:
, устанавливаем связь между отопительным и холодильным коэффициентами установки:

Так как отводимая от окружающей среды теплота  всегда отлична от нуля, то эффективность теплового насоса, в соответствии с её определением, будет больше единицы. Этот результат не противоречит второму началу термодинамики, запрещающему полное превращение тепла в работу, но не обратный процесс. Преимущество теплового насоса по сравнению с электронагревателем заключается в том, что на нагрев помещений используется не только преобразованная в теплоту электроэнергия, но и теплота, отобранная от окружающей среды. По этой причине эффективность тепловых насосов может быть гораздо выше обычных электронагревателей. [2].
всегда отлична от нуля, то эффективность теплового насоса, в соответствии с её определением, будет больше единицы. Этот результат не противоречит второму началу термодинамики, запрещающему полное превращение тепла в работу, но не обратный процесс. Преимущество теплового насоса по сравнению с электронагревателем заключается в том, что на нагрев помещений используется не только преобразованная в теплоту электроэнергия, но и теплота, отобранная от окружающей среды. По этой причине эффективность тепловых насосов может быть гораздо выше обычных электронагревателей. [2].
69 цикл Карно́ теорема Карно
В термодинамике цикл Карно́ или процесс Карно — это обратимый круговой процесс, состоящий из двух адиабатических и двух изотермических процессов[1]. В процессе Карно термодинамическая система выполняет механическую работу и обменивается теплотой с двумя тепловыми резервуарами, имеющими постоянные, но различающиеся температуры. Резервуар с более высокой температурой называется нагревателем, а с более низкой температурой — холодильником[2].
Цикл Карно назван в честь французского учёного и инженера Сади Карно, который впервые его описал в своём сочинении «О движущей силе огня и о машинах, способных развивать эту силу» в 1824 году[3][4].
Поскольку обратимые процессы могут осуществляться лишь с бесконечно малой скоростью, мощность тепловой машины в цикле Карно равна нулю. Мощность реальных тепловых машин не может быть равна нулю, поэтому реальные процессы могут приближаться к идеальному обратимому процессу Карно только с большей или меньшей степенью точности. В цикле Карно тепловая машина преобразует теплоту в работу с максимально возможным коэффициентом полезного действия из всех тепловых машин, у которых максимальная и минимальная температуры в рабочем цикле совпадают соответственно с температурами нагревателя и холодильника в цикле Карно[5].
Описание цикла Карно

Рис. 1. Цикл Карно в координатах T—S
Пусть тепловая машина состоит из нагревателя с температурой  , холодильника с температурой
, холодильника с температурой  и рабочего тела.
и рабочего тела.
Цикл Карно состоит из четырёх обратимых стадий, две из которых осуществляются при постоянной температуре (изотермически), а две — при постоянной энтропии (адиабатически). Поэтому цикл Карно удобно представить в координатах T (температура) и S (энтропия).
1. Изотермическое расширение (на рис. 1 — процесс A→Б). В начале процесса рабочее тело имеет температуру  , то есть температуру нагревателя. Затем тело приводится в контакт с нагревателем, который изотермически (при постоянной температуре) передаёт ему количество теплоты
, то есть температуру нагревателя. Затем тело приводится в контакт с нагревателем, который изотермически (при постоянной температуре) передаёт ему количество теплоты  . При этом объём рабочего тела увеличивается, оно совершает механическую работу, а его энтропия возрастает.
. При этом объём рабочего тела увеличивается, оно совершает механическую работу, а его энтропия возрастает.
2. Адиабатическое расширение (на рис. 1 — процесс Б→В). Рабочее тело отсоединяется от нагревателя и продолжает расширяться без теплообмена с окружающей средой. При этом температура тела уменьшается до температуры холодильника  , тело совершает механическую работу, а энтропия остаётся постоянной.
, тело совершает механическую работу, а энтропия остаётся постоянной.
3. Изотермическое сжатие (на рис. 1 — процесс В→Г). Рабочее тело, имеющее температуру  , приводится в контакт с холодильником и начинает изотермически сжиматься под действием внешней силы, отдавая холодильнику количество теплоты
, приводится в контакт с холодильником и начинает изотермически сжиматься под действием внешней силы, отдавая холодильнику количество теплоты  . Над телом совершается работа, его энтропия уменьшается.
. Над телом совершается работа, его энтропия уменьшается.
4. Адиабатическое сжатие (на рис. 1 — процесс Г→А). Рабочее тело отсоединяется от холодильника и сжимается под действием внешней силы без теплообмена с окружающей средой. При этом его температура увеличивается до температуры нагревателя, над телом совершается работа, его энтропия остаётся постоянной.
Теоремы Карно.
- Все обратимые машины, работающие по циклу Карно, имеют, независимо от природы рабочего тела, одинаковый КПД при условии если у них общий нагреватель и холодильник.
- Если две тепловые машины имеют общий нагреватель и холодильник и одна обратимая, а другая необратимая, то КПД обратимой больше необратимой

Уравнение политропного процесса
Политропный процесс это процесс, в котором теплоемкость остается постоянной. Политропным процессом являются изохорный, изобарный, изотермический и адиабатный процессы, потому что все они имеют общую особенность - они происходят при постоянной теплоемкости.
Политропа это график зависимости между параметрами состояния идеального газа при  . Политропа в координатах p, V - гипербола, занимающая промежуточное положение между изотермой и адиабатой.
. Политропа в координатах p, V - гипербола, занимающая промежуточное положение между изотермой и адиабатой.
Исходя из первого начала термодинамики при условии постоянства теплоемкости (  ), можно вывести уравнение политропы:
), можно вывести уравнение политропы:
 - уравнение политропы,
- уравнение политропы,
где  - показатель политропы.
- показатель политропы.
|
Просмотров 1445 |
|
|
