
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Строение. Изомерия и номенклатура
|
|
Простейшими непредельными (ненасыщенными) соединениями являются углеводороды, содержащие одну или несколько двойных связей. Алкены, содержащие две двойные связи, называются диенами, содержащие три двойные связи — триенами и т.д. Соединения с несколькими двойными связями имеют общее название полиены.
Алкенами называются непредельные углеводороды, молекулы которых содержат одну двойную связь. Первый представитель этого класса — этилен СН2 = СН2, в связи с чем алкены также называют этиленовыми углеводородами. Ближайшие гомологи этилена:
| СН3-СН=СН2 | СН3-СН2-СН=СН2 | СН3-СН=СН-СН3 |
| пропилен | бутен-1 | бутен-2 |
Простейший алкен с разветвленным углеродным скелетом:
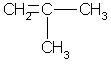
2-метил промен
Общая формула гомологического ряда алкенов СnН2n. Она совпадает с общей формулой циклоалкана, поэтому алкены и циклоалканы являются межклассовыми изомерами.
При отщеплении атома водорода от молекул алкенов образуются непредельные радикалы обшей формулы CnH2n-1, простейшие из которых — винил (этенил) иаллил (пропенил):
| СН2=СН- | СН2=СН-СН2- |
| винил | аллил |
Атомы углерода при двойной связи находятся в состоянии sp2-гибридизации. Три σ-связи, образованные гибридными орбиталями, располагаются в одной плоскости под углом 120° друг к другу; π-связь образована при перекрывании негибридных 2р-орбиталей соседних атомов углерода. При этом атомные р-орбитали перекрываются не в межъядерном пространстве, а вне его. Поэтому такое "боковое" перекрывание менее эффективно, чем осевое, и, следовательно, π-связь является менее прочной, чем σ-связь. Дополнительное π-связывание двух атомов углерода приводит к тому, что уменьшается расстояние между ядрами, поскольку двойная связь является сочетанием σ- и π-связей. Длина двойной связи С=С составляет 0.133 нм, что существенно меньше длины одинарной связи (0,154 нм). Энергия двойной связи (606 кДж/моль) меньше удвоенного значения энергии одинарной связи (347-2 = 694 кДж/моль); это обусловлено меньшей энергией π-связи.
Структурная изомерия алкенов обусловлена изомерией углеродного скелета (например, бутен-1 и 2-метилпропен) и изомерией положения двойной связи.Пространственная, или цис-транс-изомерия обусловлена различным положением заместителей относительно плоскости двойной связи.
Если каждый из атомов углерода при связи С=С связан с двумя разными заместителями, то эти заместители могут располагаться по одну сторону от плоскости двойной связи (цис-изомер) или по разные стороны (транс-изомер), например:

цис-бутен-2 транс-бутен-2
Эти два изомера нельзя перевести друг в друга без вращения вокруг двойной связи С=С, а это вращение требует разрыва π-связи и затраты большого количества энергии. Поэтому цис- и транс-изомеры представляют собой разные индивидуальные вещества, которые отличаются друг от друга физическими и химическими свойствами. Алкены, у которых хотя бы один из атомов углерода при связи С=С имеет два одинаковых заместителя, не имеют цис-транс-изомеров.
В алкенах с неразветвленной углеродной цепью нумерацию начинают с того конца, ближе к которому находится двойная связь. В названии соответствующего алкана окончание -ан заменяется на -ен. В разветвленных алкенах выбирают главную цепь так, чтобы она содержала двойную связь, даже если она при этом и не будет самой длинной. Перед названием главной цепи указывают номер атома углерода, при котором находится заместитель, и название этого заместителя. Номер после названия главной цепи указывает положение двойной связи, например:

4метилпентен -2
Физические свойства алкенов похожи на свойства алканов, хотя все они имеют несколько более низкие температуры плавления и кипения, чем соответствующие алканы. Например, пентан имеет температуру кипения 36 °С, а пентен-1 — 30 °С. При обычных условиях алкены С2 - С4 — газы. С5 – С15 — жидкости, начиная сC16 — твердые вещества. Алкены не растворимы в воде, хорошо растворимы в органических растворителях.
В природе алкены встречаются редко. Поскольку алкены являются ценным сырьем для промышленного органического синтеза, разработаны многие способы их получения.
1. Основным промышленным источником алкенов служит крекинг алканов, входящих в состав нефти:
| t | ||
| С8Н18 | → | С4Н10 + С4Н8 |
Крекинг протекает по свободнорадикальному механизму при высоких температурах (400-700 °С).
2. Другой промышленный способ получения алкенов - дегидрирование алканов:
| t, Cr2O3 | ||
| СН3-СН2-СН3 | → | СН3-СН=СН2 + Н2 |
3. В лабораторных условиях алкены получают по реакциям отщепления (элиминирования), при которых от соседних атомов углерода отщепляются два атома или две группы атомов, и образуется дополнительная π-связь. К таким реакциям относятся следующие.
1) Дегидратация спиртов происходит при их нагревании с водоотнимающими средствами, например с серной кислотой при температуре выше 150 °С:
| H2SO4 | ||
| СН3-СН2-ОН | → | СН2=СН2 + Н2О |
2) Отщепление галогеноводородов проводят при действии спиртовых растворов щелочей на моноалкилгалогениды:
| С2Н6ОН | ||
| СН3-СН2-СНВr-СН3 + КОН | → | СН3-СН=СН-СН3 + КВr + Н2О |
При отщеплении Н2O от спиртов, НВr и HCl от алкилгалогенидов атом водорода преимущественно отщепляется от того из соседних атомов углерода, который связан с наименьшим числом атомов водорода (от наименее гидрогенизированного атома углерода). Эта закономерность носит название правила Зайцева.
3) Дегалогенирование происходит при нагревании дигалогенидов, имеющих атомы галогена у соседних атомов углерода, с активными металлами:
CH2Br-CHBr-CH3 + Mg → СН2=СН-СН3 + MgВr2.
Химические свойства
Полимеризация алкенов и их производных в присутствии кислот протекает по механизму АE:
| Н* | ||
| nCH2=CHR | → | (-CH2-CHR-)n |
где R = Н, СН3, Cl, С6Н5 и т.д. Молекула CH2=CHR называется мономером, полученное соединение — полимером , число n-степень полимеризации.
Полимеризация различных производных алкенов дает ценные промышленные продукты: полиэтилен, полипропилен, поливинилхлорид и другие.
Кроме присоединения, для алкенов характерны также реакции окисления. При мягком окислении алкенов водным раствором перманганата калия (реакция Вагнера) образуются двухатомные спирты:
ЗСН2=СН2 + 2КМnО4 + 4Н2О ЗНОСН2-СН2ОН + 2MnO2↓ + 2KOH.
В результате протекания этой реакции фиолетовый раствор перманганата калия быстро обесцвечивается и выпадает коричневый осадок оксида марганца (IV). Эта реакция, как и реакция обесцвечивания бромной воды, является качественной на двойную связь. При жестком окислении алкенов кипящим раствором перманганата калия в кислой среде происходит полный разрыв двойной связи с образованием кетонов, карбоновых кислот или СО2, например:
| [О] | ||
| СН3-СН=СН-СН3 | → | 2СН3-СООН |
По продуктам окисления можно установить положение двойной связи в исходном алкене.
Как и все другие углеводороды, алкены горят, и при обильном доступе воздуха образуют диоксид углерода и воду:
СnН2n + Зn/2О2 → nСО2↑ + nН2О.
При ограниченном доступе воздуха горение алкенов может приводить к образованию монооксида углерода и воды:
СnН2n + nО2 → nCO↑ + nH2O.
Если смешать алкен с кислородом и пропустить эту смесь над нагретым до 200°С серебряным катализатором, то образуется оксид алкена (эпоксиалкан), например:

При любых температурах алкены окисляются озоном (озон более сильный окислитель, чем кислород). Если газообразный озон пропускают через раствор какого-либо алкена в тетрахлор-метане при температурах ниже комнатной, то происходит реакция присоединения, и образуются соответствующие озониды (циклические перекиси). Озониды очень неустойчивы и могут легко взрываться. Поэтому обычно их не выделяют, а сразу после получения разлагают водой — при этом образуются карбонильные соединения (альдегиды или кетоны), строение которых указывает на строение подвергавшегося озонированию алкена.
Низшие алкены — важные исходные вещества для промышленного органического синтеза. Из этилена получают этиловый спирт, полиэтилен, полистирол. Пропен используют для синтеза полипропилена, фенола, ацетона, глицерина.
Полимеризация – реакция образования высокомолекулярного соединения (полимера) путем последовательного присоединения молекул низкомолекулярного вещества (мономера) по схеме:

Число n называется степенью полимеризации. Реакции полимеризации алкенов идут в результате присоединения по кратным связям:

Димеризация алкенов – образование димера (удвоенной молекулы) в результате реакции присоединения. В присутствии минеральной кислоты (донора протона Н+) происходит присоединение протона по двойной связи молекулы алкена. При этом образуется карбокатион:
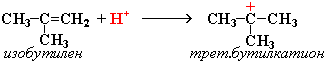
Этот карбокатион присоединяется к следующей молекуле алкена с образованием "димерного карбокатиона":

"Димерный карбокатион" стабилизируется путем выброса протона, что приводит к продуктам димеризации алкена – смеси изомерных диизобутиленов (2,4,4-триметипентена-2 и 2,4,4-триметилпентена-1):

Этот процесс протекает при обработке изобутилена (2-метипропена) 60% серной кислотой при температуре 70С. Образовавшаяся в результате смесь диизобутиленов подвергается гидрированию с целью получения "изооктана" (2,2,4-триметилпентана), который применяется для улучшения антидетонационной способности бензина ("изооктан" – стандарт моторного топлива с октановым числом 100).
Подобно реакции димеризации алкенов происходит их полимеризация, только процесс не останавливается на стадии образования димера, а идет дальше и включает в себя множество стадий присоединения молекул алкена к растущему карбокатиону.
3. Алкены. Химические свойства: реакции электрофильного присоединения (AdE). Правило Марковникова. Применение правило Марковникова в реакциях присоединения к несиметричным олефинам. Радикальный механизм присоединения (AdR) (перекисный эффект Караша).
Химические свойства алкенов определяются наличием в их молекулах двойной связи. Электронная плотность π-связи достаточно подвижна и легко вступает в реакции с электрофильными частицами. Поэтому многие реакции алкенов протекают по механизму электрофильного присоединения, обозначаемому символом AE(от англ, addition electrophilic).
Реакции злектрофильного присоединения это ионные процессы, протекающие в несколько стадий.На первой стадии электрофильная частица (чаще всего это бывает протон H+) взаимодействует с π-электронами двойной связи и образует π-комплекс, который затем превращается в карбокатион путем образования ковалентной σ-связи между электрофильной частицей и одним из атомов углерода:

алкен π-комплекс карбокатион
На второй стадии карбокатион реагирует с анионом X-, образуя вторую σ-связь за счет электронной пары аниона:

Ион водорода в реакциях электрофильного присоединения присоединяется к тому из атомов углерода при двойной связи, на котором больше отрицательный заряд.
Распределение зарядов определяется смещением π-электронной плотности под влиянием заместителей:  .
.
Электронодонорные заместители, проявляющие +I -эффект, смещают π-электронную плотность к более гидрогенизированному атому углерода и создают на нем частичный отрицательный заряд.
Этим объясняется правило Марковникова: при присоединении полярных молекул типа НХ(X= Hal, ОН, CN и т.п.) к несимметричным алкенам водород преимущественно присоединяется к более гидрогенизированному атому углерода при двойной связи.
Рассмотрим конкретные примеры реакций присоединения.
1) Гидрогалогенирование. При взаимодействии алкенов с галогеноводородами (HCl, НВr) образуются алкилгалогениды (перекисный эффект Караша) :
СН3-СН=СН2 + НВr СН3-СНВr-СН3.
Продукты реакции определяются правилом Марковникова.
Следует, однако, подчеркнуть, что в присутствии какого-либо органического пероксида полярные молекулы НХ реагируют с алкенами не по правилу Марковникова:
| R-O-O-R | ||
| СН3-СН=СН2 + НВr | → | СН3-СН2-СН2Вr |
обращает на себя тот факт, что реакция идет против правила Марковникова. такое аномальное явление называется пероксидный эффект.
Это связано с тем, что присутствие перекиси обусловливает радикальный, а не ионный механизм реакции.
Инициирование радикальной цепи:
Рост цепи:
Обрыв цепи:
Хлороводород и йодоводород не присоединяются к алкенам по радикальному механизму (только в присутствие пероксидов – перекисный эффект Караша – описан выше).
Эффект Караша (перекисный эффект) — обращение региоселективности при присоединении галогеноводородов к алкенам в присутствии кислорода или перекисей. Данный эффект, впервые описанный М. Карашем и Ф. Майо в 1933 году, заключается в образовании аномального продукта, формально не соответствующего правилу Марковникова. Это связывают с изменением механизма реакции, которая в данном случае протекает не как электрофильное присоединение, а как радикальное присоединение.

2) Гидратация. При взаимодействии алкенов с водой в присутствии минеральных кислот (серной, фосфорной) образуются спирты. Минеральные кислоты выполняют роль катализаторов и являются источниками протонов. Присоединение воды также идет по правилу Марковникова:
СН3-СН=СН2 + НОН → СН3-СН(ОН)-СН3.
3) Галогенирование. Алкены обесцвечивают бромную воду:
СН2=СН2 + Вr2 → ВrСН2-СН2Вr.
Эта реакция является качественной на двойную связь.
4) Гидрирование. Присоединение водорода происходит под действием металлических катализаторов:
| t, Ni | ||
| СН3-СН=СН2 + Н2 | → | СН3-СН2-СН3 |
5) Полимеризация алкенов и их производных в присутствии кислот протекает по механизму АE:
| Н* | ||
| nCH2=CHR | → | (-CH2-CHR-)n |
где R = Н, СН3, Cl, С6Н5 и т.д. Молекула CH2=CHR называется мономером, полученное соединение — полимером , число n-степень полимеризации.
Полимеризация различных производных алкенов дает ценные промышленные продукты: полиэтилен, полипропилен, поливинилхлорид и другие.
4. Диеновые углеводороды. Номенклатура. Три основных типа диеновых углеводородов. Способы получения сопряженных диеновых углеводородов: дивинила, изопрена. Получение дивинила по методу С.В. Лебедева.
|
Просмотров 1138 |
|
|
