
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Физический смысл универсальной газовой постоянной
|
|
 - универсальная газовая постоянная численно равна работе 1
- универсальная газовая постоянная численно равна работе 1
моля идеального газа при изобарном нагревании на 1 К.
В общем случае надо процесс разбить на малые части и сосчитать элементарные работы, а затем их сложить
(процесс интегрирования): 
Например, в изотермическом процессе 
В изохорном процессе объем не меняется, следовательно, в изохорном процессе работа не совершается!
В адиабатном процессе  .
.
2)
В теории идеального газа потенциальная энергия взаимодействия молекул считается равной нулю. Поэтому внутренняя энергия идеального газа определяется кинетической энергией движения всех его молекул. Средняя энергия движения одной молекулы равна

Так как в одном киломоле содержится  молекул, то внутренняя энергия одного киломоля газа будет
молекул, то внутренняя энергия одного киломоля газа будет

Учитывая, что  , получим
, получим

Для любой массы m газа, т.е. для любого числа киломолей 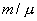 внутренняя энергия
внутренняя энергия

| (10.12) |
Из этого выражения следует, что внутренняя энергия является однозначной функцией состояния и, следовательно, при совершении системой любого процесса, в результате которого система возвращается в исходное состояние, полное изменение внутренней энергии равно нулю. Математически это записывается в виде тождества

3) В термодинамически неравновесных системах происходят особые необратимые процессы, называемые явлениями переноса, в результате которых осуществляется пространственный перенос массы, импульса, энергии. К явлениям переноса относятся теплопроводность (перенос энергии), диффузия (перенос массы) и внутреннее трение (перенос импульса). Ограничимся одномерными явлениями переноса. Систему отсчета будем выберать так, чтобы ось х была направлена в сторону в направления переноса.
1. Теплопроводность. Если в первой области газа средняя кинетическая энергия молекул больше, чем во второй, то вследствие постоянных столкновений молекул с течением времени происходит процесс выравнивания средних кинетических энергий молекул, т. е., выравнивание температур. Перенос энергии в форме теплоты подчиняется закону Фурье:
 (1)
(1)
где jE — плотность теплового потока — величина, которая определяется энергией, переносимой в форме теплоты в единицу времени через единичную площадку, перпендикулярную оси х, λ — теплопроводность, — градиент температуры, равный скорости изменения температуры на единицу длины х в направлении нормали к этой площадке. Знак минус говорит о том, что во время теплопроводности энергия перемещается в направлении убывания температуры (поэтому знаки jE и – противоположны). Теплопроводность λ равна плотности теплового потока при градиенте температуры, равном единице.
Можно показать, что
 (2)
(2)
где сV — удельная теплоемкость газа при постоянном объеме (количество теплоты, которое необходимо для нагревания 1 кг газа на 1 К при постоянном объеме), ρ — плотность газа, <ν> — средняя скорость теплового движения молекул, <l> — средняя длина свободного пробега.
2. Диффузия. При происходит самопроизвольное проникновение и перемешивание частиц двух соприкасающихся газов, жидкостей и даже твердых тел; диффузия есть обмен масс частиц этих тел, при этом явление возникает и продолжается, пока существует градиент плотности. Во времена становления молекулярно-кинетической теории по вопросу явления диффузии возникли противоречия. Поскольку молекулы перемещаются в пространстве с огромными скоростями, то диффузия должна происходить очень быстро. Если же открыть в комнате крышку сосуда с пахучим веществом, то запах распространяется довольно медленно. Но здесь нет противоречия. При атмосферном давлении молекулы обладают малой длиной свободного пробега и, при столкновениях с другими молекулами, приемущественно «стоят» на месте.
Явление диффузии для химически однородного газа подчиняется закону Фика:
 (3)
(3)
где jm — плотность потока массы — величина, определяемая массой вещества, диффундирующего в единицу времени через единичную площадку, перпендикулярную оси х, D — диффузия (коэффициент диффузии), dρ/dx — градиент плотности, который равен скорости изменения плотности на единицу длины х в направлении нормали к этой площадке. Знак минус говорит о том, что перенос массы происходит в направлении убывания плотности (поэтому знаки jm и dρ/dx противоположны). Диффузия D численно равна плотности потока массы при градиенте плотности, равном единице. Согласно кинетической теории газов,
 (4)
(4)
3. Внутреннее трение (вязкость). Суть механизма возникновения внутреннего трения между параллельными слоями газа (жидкости), которые движущутся с различными скоростями, есть в том, что из-за хаотического теплового движения осуществляется обмен молекулами между слоями, в результате чего импульс слоя, который движется быстрее, уменьшается, который движется медленнее — увеличивается, что приводит к торможению слоя, который движется быстрее, и ускорению слоя, который движется медленнее.
Как известно, сила внутреннего трения между двумя слоями газа (жидкости) подчиняется закону Ньютона:
 (5)
(5)
где η — динамическая вязкость (вязкость), dν/dx — градиент скорости, который показывает быстроту изменения скорости в направлении х, перпендикулярном направлению движения слоев, S — площадь, на которую действует сила F.
Согласно второму закону Ньютона взаимодействие двух слоев можно рассматривать как процесс, при котором в единицу времени от одного слоя к другому передается импульс, который по модулю равен действующей силе. Тогда выражение (5) можно записать в виде
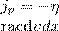 (6)
(6)
где jp — плотность потока импульса — величина, которая определяется определяемая полным импульсом, переносимым в единицу времени в положительном направлении оси х через единичную площадку, перпендикулярную оси х, dν/dx — градиент скорости. Знак минус говорит о том, что импульс переносится в направлении убывания скорости (поэтому знаки jp и dν/dx противоположны).
Динамическая вязкость η численно равна плотности потока импульса при градиенте скорости, равном единице; она вычисляется по формуле
 (7)
(7)
4)Физи́ческая кине́тика (др.-греч. κίνησις — движение) — микроскопическая теория процессов в неравновесных средах. В кинетике методами квантовой или классической статистической физики изучают процессы переноса энергии, импульса, заряда и вещества в различных физических системах (газах, плазме, жидкостях, твёрдых телах) и влияние на них внешних полей. В отличие от термодинамики неравновесных процессов и электродинамики сплошных сред, кинетика исходит из представления о молекулярном строении рассматриваемых сред, что позволяет вычислить из первых принципов кинетические коэффициенты, диэлектрические и магнитные проницаемости и другие характеристики сплошных сред. Физическая кинетика включает в себя кинетическую теорию газов из нейтральных атомов или молекул, статистическую теорию неравновесных процессов в плазме, теорию явлений переноса в твёрдых телах (диэлектриках, металлах и полупроводниках) и жидкостях, кинетику магнитных процессов и теорию кинетических явлений, связанных с прохождением быстрых частиц через вещество. К ней же относятся теория процессов переноса в квантовых жидкостях и сверхпроводниках и кинетика фазовых переходов.
Если известна функция распределения всех частиц системы по их координатам и импульсам в зависимости от времени (в квантовом случае — матрица плотности), то можно вычислить все характеристики неравновесной системы. Вычисление полной функции распределения является практически неразрешимой задачей, но для определения многих свойств физических систем, например, потока энергии или импульса, достаточно знать функцию распределения небольшого числа частиц, а для газов малой плотности — одной частицы.
В кинетике используется существенное различие времён релаксации в неравновесных процессах; например, для газа из частиц или квазичастиц, время свободного пробега значительно больше времени столкновения между частицами. Это позволяет перейти от полного описания неравновесного состояния функцией распределения по всем координатам и импульсам к сокращённому описанию при помощи функции распределения одной частицы по её координатам и импульсам.
Основной метод физической кинетики — решение кинетического уравнения Больцмана для одночастичной функции распределения  молекул в фазовом пространстве их координат x и импульсов p. Функция распределения удовлетворяет кинетическому уравнению:
молекул в фазовом пространстве их координат x и импульсов p. Функция распределения удовлетворяет кинетическому уравнению:

где St — интеграл столкновений, определяющий разность числа частиц, приходящих в элемент объёма вследствие прямых столкновений и убывающих из него вследствие обратных столкновений. Для одноатомных молекул или для многоатомных, но без учёта их внутренних степеней свободы

где ω — вероятность столкновения, связанная с дифференциальным эффективным сечением рассеяния.

где p, p1 — импульсы молекул до столкновения, v, v1 — соответственно скорости, p', p'1 — их импульсы после столкновения, f, f1 — функции распределения молекул до столкновения, f', f'1 — их функции распределения после столкновения.
Для газа из сложных молекул, обладающих внутренними степенями свободы, их следует учитывать в функции распределения. Например, для двухатомных молекул с собственным моментом вращения M функции распределения будут зависеть также от M.
Из кинетического уравнения следует теорема Больцмана — убывание со временем H-функции Больцмана (среднего логарифма функции распределения) или возрастание энтропии, так как она равна H-функции Больцмана с обратным знаком.
5) Термодинамика основывается на трёх законах — началах, которые сформулированы на основе экспериментальных данных и поэтому могут быть приняты как постулаты.
1-й закон — первое начало термодинамики. Представляет собой формулировку обобщённого закона сохранения энергии для термодинамических процессов. В наиболее простой форме его можно записать как δQ = δA + dU, где dU есть полный дифференциал внутренней энергии системы, а δQ и δA есть элементарное количество теплоты, переданное системе, и элементарная работа, совершенная системой соответственно. Нужно учитывать, что δA и δQ нельзя считать дифференциалами в обычном смысле этого понятия
При изобарном нагревании газ совершает работу над внешними силами 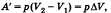 , где V1 и V2 — начальный и конечный объемы газа. Если процесс не является изобарным, величина работы может быть определена площадью фигуры ABCD, заключенной между линией, выражающей зависимость p(V), и начальным и конечным объемами газа V
, где V1 и V2 — начальный и конечный объемы газа. Если процесс не является изобарным, величина работы может быть определена площадью фигуры ABCD, заключенной между линией, выражающей зависимость p(V), и начальным и конечным объемами газа V

Рассмотрим применение первого закона термодинамики к изопроцессам, происходящим с идеальным газом.
В изотермическом процессе температура постоянная, следовательно, внутренняя энергия не меняется. Тогда уравнение первого закона термодинамики примет вид:  , т. е. количество теплоты, переданное системе, идет на совершение работы при изотермическом расширении, именно поэтому температура не изменяется.
, т. е. количество теплоты, переданное системе, идет на совершение работы при изотермическом расширении, именно поэтому температура не изменяется.
В изобарном процессе газ расширяется и количество теплоты, переданное газу, идет на увеличение его внутренней энергии и на совершение им работы:  .
.
При изохорном процессе газ не меняет своего объема, следовательно, работа им не совершается, т. е. А = 0, и уравнение первого закона имеет вид  , т. е. переданное количество теплоты идет на увеличение внутренней энергии газа.
, т. е. переданное количество теплоты идет на увеличение внутренней энергии газа.
Адиабатным называют процесс, протекающий без теплообмена с окружающей средой. Q = 0, следовательно, газ при расширении совершает работу за счет уменьшения его внутренней энергии, следовательно, газ охлаждается,  Кривая, изображающая адиабатный процесс, называется адиабатой.
Кривая, изображающая адиабатный процесс, называется адиабатой.
, поскольку эти величины существенно зависят от типа процесса, в результате которого состояние системы изменилось.
6) молекулы многоатомных газов нельзя рассматривать как материальные точки. Необходимо учитывать вращательное движение молекул и число степеней свободы этих молекул.
Числом степени свободы (i) называется число независимых переменных, определяющих положение тела в пространстве.
Положение одноатомной молекулы, как и материальной точки, задаётся тремя координатами, поэтому она имеет три степени свободы (рис. 4.3).
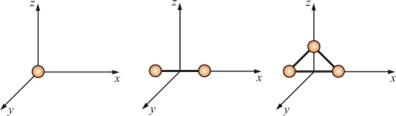
Рис. 4.3
Многоатомная молекула может ещё и вращаться. Например, у двухатомных молекул вращательное движение можно разложить на два независимых вращения, а любое вращение можно разложить на три вращательных движения вокруг взаимно перпендикулярных осей. Но для двухатомной молекулы вращение вокруг её собственной оси не изменит её положение в пространстве, а момент инерции относительно этой оси равен нулю (рис. 4.3).
Таким образом, у двухатомных молекул пять степеней свободы (i = 5), а у трёхатомных шесть степеней свободы (i = 6).
При взаимных столкновениях молекул возможен обмен их энергиями и превращение энергии вращательного движения в энергию поступательного движения и обратно. Таким путём было установлено равновесие между значениями средних энергий поступательного и вращательного движения молекул. Больцман доказал, что для не слишком низких температур средняя энергия  , приходящаяся на одну степень свободы, равна
, приходящаяся на одну степень свободы, равна 
6) теплоемкость тела – это величина, характеризующая способность тела изменять свою температуру с подводом или отводом теплоты. Она равна количеству теплоты, которое надо подвести к телу, чтобы изменить его температуру на 1 К:
 ,
,  Дж / К,
Дж / К,
в дифференциальной форме, т. е. при подводе элементарного количества тепла:
 .
.
Чтобы теплоемкость являлась физической характеристикой того или иного вещества, ее измерение необходимо проводить в одних и тех же условиях. Обычно экспериментальные измерения теплоемкостей проводят при р=const, V=const и определяют соответственно изобарную ср и изохорную сv теплоемкости. Разность между этими теплоемкостями для идеального газа, в соответствии с известной из физики формулой Майера, равна:
 ,
,
а отношение теплоемкостей
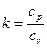
называется показателем адиабаты. Из молекулярно-кинетической теории идеальных газов известны численные значения показателя адиабаты, они зависят от числа атомов в молекуле газа:
- одноатомный газ k = 1,67;
- двухатомный газ k = 1,4;
- трех- и многоатомный газ k = 1,33.
7) Классическая теория теплоемкости основана на предполо-
ожении, что к атомно-молекулярным системам применимы законы
классической ньютоновой механики. В действительности примени-
мость ньютоновой механики к атомно-молекулярным системам
ограничена. По этой причине классическая теория не смогла дать
полного удовлетворительного решения проблемы теплоемкости и
была заменена более общей квантовой теорией. Однако во многих
случаях классическая теория приводила к удивительно хорошему
согласию с опытом. Причина этого в том, что классическая теория
является приближенным предельным случаем квантовой и, следо-
вательно, имеет определенную область применимости. В пределах
этой области выводы классической теории практически не отли-
чаются от выводов квантовой. Мы начинаем изложение с класси-
ческой теории. Она проще квантовой. При таком порядке изложе-
ния отчетливее выявятся принципиальные затруднения класси-
ческой физики, преодоление которых привело к замене классиче-
ских представлений квантовыми.
Для классических систем справедлива теорема о равномерном распределении кинетической энергии по степеням свободы. На основе этой теоремы можно построить классическую теорию теплоемкостей газов и твердых тел. Начнем с теплоемкости газов. В § 24 было показано, что для идеальных газов
cv = v Cp = v£i- (66-1)
Отсюда видно, что адиабатическая постоянная у однозначно определяет обе теплоемкости СР и Cv идеального газа. Поэтому для сопоставления теории с опытом достаточно сравнивать между собой опытные и теоретические значения только адиабатической постоянной у.
Внутренняя энергия газа состоит из кинетической энергии поступательного, вращательного и внутреннего движения молекул и атомов, а также из потенциальной энергии их взаимодействия. Для идеальных газов, когда молекулярные силы пренебрежимо малы, потенциальной энергией взаимодействия молекул можно пренебречь.
8)Второе начало термодинамики — физический принцип, накладывающий ограничение на направление процессов передачи тепла между телами.
Второе начало термодинамики гласит, что невозможен самопроизвольный переход тепла от тела, менее нагретого, к телу, более нагретому.
Второе начало термодинамики запрещает так называемые вечные двигатели второго рода, показывая что коэффициент полезного действия не может равняться единице, поскольку для кругового процесса температура холодильника не должна равняться 0.
Второе начало термодинамики является постулатом, не доказываемым в рамках термодинамики. Оно было создано на основе обобщения опытных фактов и получило многочисленные экспериментальные подтверждения.
9)Третье начало термодинамики может быть сформулировано так:
«Приращение энтропии при абсолютном нуле температуры стремится к конечному пределу, не зависящему от того, в каком равновесном состоянии находится система».
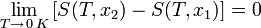
или

где x — любой термодинамический параметр.
Третье начало термодинамики относится только к равновесным состояниям.
Поскольку на основе второго начала термодинамики энтропию можно определить только с точностью до произвольной аддитивной постоянной (то есть, определяется не сама энтропия, а только её изменение):
 ,
,
третье начало термодинамики может быть использовано для точного определения энтропии. При этом энтропию равновесной системы при абсолютном нуле температуры считают равной нулю.
Третье начало термодинамики позволяет находить абсолютное значение энтропии, что нельзя сделать в рамках классической термодинамики (на основе первого и второго начал термодинамики). В классической термодинамике энтропия может быть определена лишь с точностью до произвольной аддитивной постоянной S0, что не мешает термодинамическим исследованиям, так как реально измеряется разность энтропий (S0) в различных состояниях.
10). Изменение энтропии в изопроцессах. Энтропия системы является функцией ее состояния, определенная с точностью до произвольной постоянной. Если система совершает равновесный переход из состояния 1 в состояние 2, то изменение энтропии:

|
Просмотров 1438 |
|
|
