
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Растворимость газов в жидкостях. Закон Генри. Закон Дальтона. Закон распределения
|
|
Растворимость с повышением температуры уменьшается. Также зависит от давления, под которым газ находится в жидкости.
Закон Генри: растворимость газа, выраженная в весовых единицах, при постоянной температуре пропорциональна давлению газа над раствором.
Скорость перехода газа в раствор: 

Закон обычно записывают:  Г – константа Генри.
Г – константа Генри.
Закону подчиняются газы, растворимость которых невелика и которые не вступают в реакцию с срастворителем (т.е. идеальный раствор).
Если записать закон как  получим зависимость парциального давления от концентрации в растворе.
получим зависимость парциального давления от концентрации в растворе.
Для некоторых газов справедлив закон Сивертса  n уменьшается с ростом температуры.
n уменьшается с ростом температуры.
Растворимость газа обычно указывается в миллилитрах, растворяющихся в 100 мл растворителя при данной температуре.
______________________________________
Закон Дальтона: в случае растворения смеси газов в жидкости каждый из них растворяется пропорционально своему парциальному давлению.
Примечание автора. Закон Дальтона – фактически следствие закона Генри.
________________________________________
Закон распределения.
Если при постоянной температуре некоторое вещество распределяется между двумя соприкасающимися фазами, то отношение концентрации этого вещества в соприкасающихся фазах есть величина постоянная – коэффициент растворения L.
Величина L не зависит от количества вводимого третьего вещества, а определяется природой фаз 1,2 и природой третьего вещества.
 Можно сказать, что закон Генри – частный случай закона распределения.
Можно сказать, что закон Генри – частный случай закона распределения.
Закон распределения применяется в технике (экстракция стали из шлака), при глубокой очистке полупроводниковых материалов (метод плавки по закону распределения).
Скорость гетерогенной химической реакции.
Гетерогенные (многофазные) реакции происходят на поверхности раздела соприкасающихся фаз. Сюда относятся такие процессы, как горение топлива, окисление металлов кислородом воздуха, растворение газа в жидкостях.
Скорость реакций зависит от размеров и состояния поверхности раздела фаз.
Гетерогенные процессы многостадийны. Кроме основного процесса, обязательны стадии подвода к
этой поверхности исходных веществ и отвода от нее продуктов реакции.
Если определяющей стадией является химическая реакция на поверхности раздела фаз, то процесс описывается законами химической кинетики (протекает в кинетической области).
Если, как это обычно бывает, наиболее медленно совершается подвод и отвод, то процесс описывается законами диффузии (протекает в диффузионной области).
Температура сильнее влияет на скорость химической реакции, нежели на коэффициент диффузии. Так, повышение температуры на каждые 10 градусов увеличивает коэффициент диффузии на 20%, тогда как скорость реакции увеличивается в 2-4 раза.
Диффузия оказывает большое влияние на протекание гетерогенных процессов.
Первый закон диффузии.
Масса веществ  переносимого путем диффузии в направлении х через перпендикулярную этому направлению площадку, пропорциональна коэффициенту диффузии D, площади S, времени
переносимого путем диффузии в направлении х через перпендикулярную этому направлению площадку, пропорциональна коэффициенту диффузии D, площади S, времени  и градиенту концентрации
и градиенту концентрации 

Скорость диффузии 

Знак «-» указывает, что процесс диффузии направлен в сторону понижения концентрации.
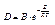 Е – энергия активации.
Е – энергия активации.
Второй закон диффузиивыражает зависимость изменения концентрации в объеме одной из соприкасающихся фаз от времени: 
___________________________________________
Стационарная диффузия.
При СД концентрация меняется только с расстоянием (х), от времени – нет. 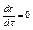
=> 
 а – градиент концентрации.
а – градиент концентрации.
Эффективный путь диффузии.
при




 толщина диффузионного слоя.
толщина диффузионного слоя.
|
Просмотров 1138 |
|
|
