
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

IV. Аналитические, качественные реакции аминокислот и пептидов
|
|
Многие качественные реакции в настоящее время для обнаружения
a-аминокислот и пептидов.
1. Способность к образованию комплексных солей с ионами тяжелых металлов:
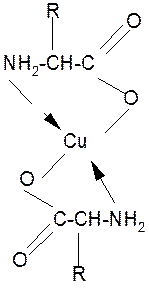 |
··
 2NH2-CH-C=O + Cu2+ +2Н+
2NH2-CH-C=O + Cu2+ +2Н+
½ ½
R OH
··
Комплексная соль Cu2+ хорошо растворима в воде и окрашена в ярко-синий цвет, что может быть использовано как качественная реакция на a- аминокислоты.
2. Образование оснований Шиффа:

 H-C=O + H2N-CH2-COOH H2C-NH-CH2-COOH H2O +
H-C=O + H2N-CH2-COOH H2C-NH-CH2-COOH H2O +
½ глицин ½
H OH
+ CH2=N-CH2-COOH
метилениминокислота
Реакция лежит в основе метода формольного титрования по Зеренсену. Сами аминокислоты вследствие амфотерности не могут быть оттитрованы щелочью. Иминокислота содержит свободную карбоксильную группу и может быть определена количественно титрованием щелочью.
3. Взаимодействие с 2,4-динитрофторбензолом – ДНФБ (реактивом Сенджера):
 | |||
 | |||
 + H2N-CH-COOH
+ H2N-CH-COOH
½ –HF
R
ДНФБ a-аминокислота ДНБ-производное
ДНБ-производное аминокислоты может быть выделено и идентифицировано хроматографически. Метод служит для определения аминокислотной последовательности белка.
4. Нингидриновая реакция обусловлена наличием a- аминогруппы, качественная реакция на a- аминокислоты, пептиды и белки:
 t°
t°
 + NH2-CH-COOH
+ NH2-CH-COOH
2 ½
R
a- аминокислота
нингидрин
 |
 H + CO2 + 3H2O + R-CHO
H + CO2 + 3H2O + R-CHO
продукт сине-фиолетового цвета
Глоссарий
Амфотерность – способность соединения проявлять и кислотные, и основные свойства.
Первичная структура пептидов и белков – это аминокислотная последовательность, т.е. порядок чередования a-аминокислотных остатков в молекуле.
Вторичная структура пептидов и белков – это пространственная ориентация основной полипептидной цепи. Основные виды - a- спираль и b–структура.
Изоэлектрическое состояние молекулы – состояние молекулы аминокислоты, пептида или белка, при котором суммарный заряд на молекуле равен нулю.
Изоэлектрическая точка – значение рН водного раствора аминокислоты, пептида или белка, при котором молекула достигает изоэлектрического состояния.
Пептидная связь (группа) – это группа атомов -СО–NН - , регулярно повторяющаяся в полимерной цепи молекулы.
Тема 8. Углеводы
Цель занятия: закрепить и расширить знания принципов стереоизомерии, таутомерного равновесия и химических свойств, важнейших моно-, ди- и полисахаридов, участвующих в процессах жизнедеятельности, а также приобрести практические навыки идентификации углеводов.
Конкретные задачи
1. Студент должен знать:
– пространственное строение моно-, ди- и полисахаридов;
– виды изомерии и таутомерию углеводов, а также их химические свойства и биологическое значение.
2. Студент должен уметь:
– писать формулы важнейших моно-, ди- и полисахаридов в открытой и циклической формах;
– изображать конформации пиранозного цикла моносахаридов и фрагментов полисахаридов;
– определять по формуле Фишера принадлежность углевода к стереохимическому ряду (D - или L -);
– описывать уравнениями химические свойства моносахаридов;
– доказывать восстанавливающую способность углеводов дисахаридов;
– проводить качественные реакции для обнаружения и доказательства строения глюкозы, фруктозы, мальтозы, сахарозы, крахмала.
Мотивация. Углеводы – один из важнейших классов органических природных соединений, играющий большую роль в процессах, обеспечивающих нормальную деятельность живых организмов. Они принимают участие в энергетическом и пластическом обмене; с углеводами связана специфичность групп крови высших организмов; химия иммунитета. Многие углеводы используются в качестве медицинских препаратов.
Вопросы для самоподготовки
1. Открытые и циклические таутомерные формы глюкозы, галактозы, маннозы,
фруктозы, рибозы, дезоксирибозы и ксилозы.
2. Реакции окисления и восстановления моносахаридов.
3. Гликозиды и их биологическая роль.
4. Сложные эфиры углеводов: моно-, ди- и полисахаридов.
5. Доказательство строения углеводов – моносахаридов.
6. Строение, номенклатура и восстанавливающая способность дисахаридов:
мальтозы, лактозы, целлобиозы.
7. Строение гомополисахаридов: крахмала, гликогена, клетчатки (целлюлозы). Их
гидролиз.
|
Просмотров 879 |
|
|
