
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Цвета растворов и соответствующих им светофильтров 3 часть
|
|
4.2. ХРОМАТОГРАФИЧЕСКИЕ ПАРАМЕТРЫ
На рис.16 представлена идеализированная хроматограмма смеси двух веществ. По оси абсцисс отложено время хроматографирования (объем подвижной фазы), по оси ординат – аналитический сигнал, зависящий от концентрации веществ в элюенте (отклик).
Нулевая линия – часть хроматограммы, полученная при регистрации сигнала детектора во время выхода из колонки чистой подвижной фазы (до выхода анализируемого вещества);
w – ширина пика – отрезок, отсекаемый на нулевой линии касательными к кривой в точках перегиба;
w0,5 – расстояние между контурами пика на середине его высоты.
Символы tR1 (VR1); tR2(VR2); tR0(VR0) обозначают время (объем) удерживания определяемых и несорбирующегося компонентов соответственно.


Средством выражения результатов хроматографического разделения смеси веществ служат параметры хроматографической кривой – параметры удерживания.
Время удерживания (tR)– времяот момента ввода пробы в хроматографическую колонку до момента выхода из нее максимальной концентрации определяемого вещества. Время удерживания складывается из двух составляющих – времени пребывания вещества в подвижной tR0 и неподвижной tRs фазах: tR = tR0 tRs ( 4.1)
Значение tR0 фактически равно времени прохождения через колонку несорбируемого компонента. Несорбируемый газ вводят непосредственно перед дозированием анализируемого образца. Коэффициент распределения этого газа очень мал по сравнению с его значением для других компонентов. Обычно при работе с катарометром для этой цели используют азот, воздух.
Значение tR не зависит от количества пробы, но зависит от природы вещества и сорбента, а также упаковки сорбента и может меняться от колонки к колонке. Поэтому для характеристики истинной удерживающей способности следует ввести приведённое (исправленное) время удерживания tRІ :
tRІ =tR – tR0(4.2 )
Время удерживания (с или мин) измеряют с помощью секундомера или электронного интегратора.
4.3. КАЧЕСТВЕННЫЙ АНАЛИЗ
Качественный анализ проводится методом относительного (приведенного) времени удерживания или с помощью веществ-свидетелей.
На рис.15 изображена типичная хроматограмма анализируемой смеси, состоящей из трех компонентов. На хроматограмме каждому компоненту анализируемой пробы соответствует пик.
При сохранении в ходе опыта постоянными температуры колонки (изотермическая хроматография) и скорости газа-носителя основной качественной характеристикой является время удерживания (tR)анализируемого вещества (рис.17).
Времена удерживания могут быть использованы для качественной характеристики соединения лишь при проведении анализа в строго заданных условиях на одном и том же приборе.
На величинувремени удерживания влияют следующие факторы:
• состав, свойства и количество неподвижной фазы (твердый носитель и нанесенный на него растворитель);
• условия проведения опыта – температура колонки и скорость газа-носителя;
• конструктивные особенности используемой аппаратуры;
метод дозирования и величина дозы;
• природа газа-носителя, а также перепад давлений газа-носителя на входе и выходе колонки.
Совпадение величин удерживания неизвестного и стандартного соединений свидетельствует о том, что эти соединения могут быть идентичными.
Существует несколько вариантов идентификации на основе времени удерживания.
Один из вариантов состоит в сравнении анализируемой и эталонной смесей в одинаковых условиях.
Равенство времен удерживания пиков соответствующих компонентов обеих смесей может служить основанием идентификации. На рис.18 представлены хроматограммы испытуемой (а) и эталонной (б) смесей, полученные в одинаковых условиях.
 | |||||||
 | |||||||
 | |||||||
 | |||||||
a) б)
| |
Равенство времен удерживания анализируемого и эталонного веществ при сопоставлении хроматограмм позволяет сделать вывод о присутствии в анализируемой смеси метанола и этанола.
Другой вариант (метод метки, добавки) заключается в том, что в исследуемую смесь вводят эталонный компонент, наличие которого в этой смеси предполагается. Например, в разделяемой смеси необходимо контролировать присутствие метанола. По методу метки в данном случае снимают хроматограмму анализируемого образца (а), затем добавляют к нему для отождествления пика метанола стандарт метанола и получают повторную хроматограмму (б) (рис.19). Сопоставляя обе хроматограммы, обнаруживают, что на повторной хроматрграмме (б) пик компонента с временем удерживания 3,5 мин значительно увеличился
Следовательно, можно сделать вывод, что метанол в анализируемом образце присутствует, но в небольшом количестве.
  | |||||
 | |||||
 | |||||
4.4. КОЛИЧЕСТВЕННЫЙ АНАЛИЗ
Велика потребность в выполнении количественных газохроматографических анализов в практике научно-исследовательских, заводских и территориальных контрольно-аналитических лабораторий.
Количественный газохроматографический анализ позволяет:
определять содержание одного, нескольких или всех компонентов в многокомпонентной смеси;
определять суммарное содержание групп из нескольких компонентов, объединяемых каким-либо общим признаком;
определять микропримеси в индивидуальных химических соединениях.
Основным параметром хроматограммы, характеризующим количество анализируемого компонента, является площадь пика (S).
Для определения площадей пиков существует несколько приемов. В современных приборах площади пиков определяются с помощью интеграторов.
Существует три основных метода количественного анализа: метод абсолютной градуировки, метод внутренней нормализации и метод внутреннего стандарта.
4.4.1. Метод абсолютной градуировки
Методом абсолютной градуировки чаще всего пользуются когда нужно определять не все компоненты определяемой смеси, а только один или два, например, при анализе примесей. По этому методу получают хроматограммы определенных количеств известного соединения и строят градуировочный график (рис.20), на одной из осей которого откладывают высоты (или площади) пиков, а на другой – количество введенного вещества (q). Затем на хроматографическую колонку подают точное количество смеси неизвестного состава, измеряют высоту (или площадь) пика определяемого компонента и по градуировочному графику рассчитывают его количество(qi).
 | |||
|
Если зависимость на рисунке 20 линейна, то можно вычислить угловой коэффициент K (градуировочный множитель) и определить содержание i-го вещества (%) в пробе по формуле:
 |
где Wi – массовая доля определяемого компонента, %;
qi – величина пробы, мкл или мкг;
Ki – градуировачный множитель;
hi(si) – высота (площадь) пика, мм (мм2).
Необходимым условием реализации метода абсолютной градуировки является соблюдение строго одинаковых условий градуировки и измерений. Наиболее существенными факторами являются точность и воспроизводимость дозирования пробы. Условия хроматографирования (включая режим работы детектора и обработку результатов) должны быть идентичными.
Этот простой и точный метод является основным методом определения микропримесей.
4.4.2. Метод внутренней нормализации
Представим себе идеализированный случай: на хроматограмме зафиксированы три компонента (А, В, С), присутствующие в анализируемой пробе (рис.21).
  |
Сигнал детектора линеен во всем диапазоне концентраций, а чувствительность детектора одинакова по отношению ко всем компонентам пробы.
В методепростой нормировки сумму площадей всех пиков
SА + SВ + SС принимают за 100%, тогда отношение площади одного пика к сумме площадей, умноженное на 100%, будет характеризовать массовую долю (%) компонента смеси: WА(%) =  ;
;
WВ(%)=  ; WС(%) =
; WС(%) =  ,
,
где WА, WВ, WС – массовые доли компонентов А, В, С, соответственно, в процентах.
Этот метод основан на том предположении, что вещества, взятые в одинаковом количестве, дают одну и ту же площадь пика, независимо от их строения. Это приближенно выполняется, если вещества химически сходны, а в качестве газа-носителя применяется газ с высокой теплопроводностью (водород или гелий). Метод простой нормировки не дает точных результатов в случае различной чувствительности детектора по отношению к разделяемым компонентам смеси.
На учете различия чувствительности детектора по отношению к компонентам анализируемой смеси веществ А, В, С основан метод нормировки с градуировочными коэффициентами,и поэтому он более надежен, чем предыдущий. В этом случае расчет ведут по формуле:
Wi(%) =  ,
,
где Ki – градуировочный коэффициент i-го компонента, который определяют экспериментально или используют литературные данные.
Например, массовая доля в процентах компонента А рассчитывается по формуле:
WА(%) = 
4.4.3. Метод внутреннего стандарта
Этот метод известен под названием относительной или косвенной градуировки и основан на введении в анализируемую смесь точно известного количества стандартного вещества, не входящего в состав анализируемой пробы и дающего отдельно регистрируемый на хроматограмме последний пик. В качестве стандартного вещества выбирают вещество, удовлетворяющее следующим требованиям:
● оно должно проявляться на хроматограмме в виде пика, хорошо отделенного от остальных пиков; его пик должен стоять на хроматограмме недалеко от веществ, представляющих интерес;
● иметь концентрацию, близкую к концентрации исследуемого компонента;
● иметь строение, близкое к строению исследуемого компанента.
Так, при определении процентного содержания примеси этанола в лекарственных средствах в качестве внутреннего стандарта часто используют изопропанол, гексанол и др.
Метод внутреннего стандарта используют, если при анализе многокомпонентной смеси необходимо определить содержание одного или двух компонентов (чтобы не подсчитывать площади всех пиков).
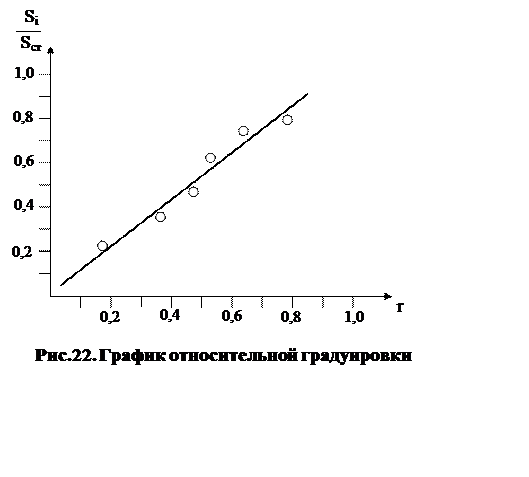 Вначале по методу внутреннего стандарта хроматографируют специально приготовленные смеси с известным весовым соотношением анализируемого вещества и стандарта и измеряют площади пиков. Затем строят зависимость отношения площадей пиков от величины весового соотношения компонента и стандарта в смеси (рис.21). После хроматографирования измеряют площади пиков анализируемого компонента (Si) и стандартного вещества (Sст).
Вначале по методу внутреннего стандарта хроматографируют специально приготовленные смеси с известным весовым соотношением анализируемого вещества и стандарта и измеряют площади пиков. Затем строят зависимость отношения площадей пиков от величины весового соотношения компонента и стандарта в смеси (рис.21). После хроматографирования измеряют площади пиков анализируемого компонента (Si) и стандартного вещества (Sст).
 |  | ||
Массовую долю анализируемого компонента Wi(%) рассчитывают по формуле:
где r – отношение массы внутреннего стандарта в смеси к массе
анализируемого вещества ;
Кi, KCT, Si, SCT – градуировочные коэффициенты, площади анализируемого компонента и стандартного вещества.
Основной недостаток указанного метода заключается в трудности подбора стандарта, не мешающего определению интересующего вещества.
Метод внутреннего стандарта обладает хорошей воспроизводимостью, высокой точностью, он не требует знания коэффициента чувствительности детектора, так как любое изменение чувствительности не оказывает влияния на величину отношения площадей.
 4.5. НЕКОТОРЫЕ СВЕДЕНИЯ О ХРОМАТОГРАФИЧЕСКИХ ПРИБОРАХ
4.5. НЕКОТОРЫЕ СВЕДЕНИЯ О ХРОМАТОГРАФИЧЕСКИХ ПРИБОРАХ
Первое сообщение о стандартном хроматографическом приборе появилось в 1943 году (этот прибор нашел применение для контроля производства синтетического каучука). Серийное производство лабораторных хроматографов началось в 1955 году, когда несколько американских фирм («Perkin Elmer», «Burrel Corp.», «Reco» и др.) практически одновременно выпустили хроматографы. С 1958 года начинается выпуск отечественных хроматографов. В настоящее время у нас широко используются хроматографы: «Кристалл 2000 М», «Кристалл 5000» (Хроматек-Кристалл, Россия), «Agilent 7890»(фирмы «Agilent Technologies», США), TRAGE GC-2000 (фирмы «Thermo scientitic», США), GC-2014 (фирмы «Shimadzu», Япония) и др.
На рисунке 23 представлен внешний вид газового хроматографа «Кристалл 2000 М».
Хроматограф «Кристалл 2000 М» позволяет:
- одновременно работать с двумя колонками различных типов: капиллярными и насадочными;
- одновременное четырёхканальное детектирование с автоматическим перераспределением потока элюата между детекторами;
- использовать полный набор детекторов;
- полностью автоматизировать анализ от ввода пробы, контроля параметров работы до обработки получаемой информации и получения результатов анализа в виде документов;
- обрабатывать и хранить информацию с нескольких хроматографов.
 |
Рис.23. Внешний вид хроматографа « Кристалл 2000М »
Хроматограф «Agilent 7890»(внешний вид представлен на рисунке 24)может быть оснащен целым рядом детекторов. Катарометр – универсальный детектор для всех веществ; пламенно-ионизационный – универсальный детектор для органических веществ; электронно-захватный – используется для обнаружения микропримесей пестицидов и гербицидов; пламенно-фотометрический – используется для обнаружения серы, фосфора (анализ загрязнений окружающей среды и биохимических объектов), масс-селективный.
Работа хроматографа определена длинным перечнем заданных параметров (температура, время, выбираемые сигналы и т.д.). Эти параметры распределены по управляющим таблицам, на которые с помощью видеоиндикаторов выводятся параметры термостата детектора и т.д.
Программное обеспечение фиксации времён удерживания (Retention Time Locking, RTL) осуществляется вплоть до тысячных долей минуты. RTL даёт возможность более легко и точно идентифицировать пики, делать больше за меньшее время, уменьшает риск недостоверных результатов и снижает эксплутационные расходы.

Рис. 24. Внешний вид газового хроматографа«Agilent 7890»
Программное обеспечение фиксации времён удерживания (Retention Time Locking, RTL) осуществляется вплоть до тысячных долей минуты. RTL даёт возможность более легко и точно идентифицировать пики, осуществлять значительно больше операций за меньшее время, уменьшает риск недостоверных результатов и снижает эксплутационные расходы.
В качестве примеров использования ГЖХ в анализе лекарственных средств в Приложении 2 представлены:
методика определения метанола и других летучих примесей в спирте этиловом 95%(Россия) согласно ФС , хроматограмма и паспорт анализа ;
методика определение органических летучих примесей в препарате эналаприла малеатв лекарственной форме порошок-субстанция (Индия) согласно НД и хроматограмма;
методика испытания на подлинность препарата масло облепиховое(Россия) согласно ФС и хроматограмма.
ВОПРОСЫ ДЛЯ САМОСТОЯТЕЛЬНОЙ ПОДГОТОВКИ
1. Какое явление лежит в основе ГЖХ?
2. Какие процессы протекают в хроматографической колонке?
3. Какова блок-схема современного газового хроматографа, укажите основные узлы.
4. Какова система подготовки газов?
5. Каким образом вводят анализируемые пробы в хроматографическую колонку?
6. Какие существуют виды аналитических колонок и их устройство?
7. Укажите назначение твердого носителя. Какие вещества используются для этого?
8. Какие вещества используются в качестве неподвижной фазы?
9. Каково функциональное назначение неподвижных фаз?
10. Каков характер температурного режима хроматографического процесса?
11. Какие детекторы входят в комплект современного хроматографа?
12.Каковы устройство и работа детектора по теплопроводности
и ПИД ?
13. Охарактеризуйте критерии хроматографического разделения:
эффективность; разрешение; селективность.
14. Укажите, каковы основные характеристики хроматограммы, используемые для идентификации анализируемых веществ, и поясните их?
15. Какие факторы влияют на величину объема и время удерживания?
16. Какие величины используют при количественной расшифровке хроматограммы?
17. Каким образом устанавливают площадь пика?
18. Какова характеристика основных методов количественного анализа?:
метод абсолютной градуировки;
метод внутренней нормализации;
метод внутреннего стандарта.
19. Каковы преимущества и недостатки газо-жидкостной хроматографии?
20. Укажите известные марки современных газовых хроматографов.
ТЕСТОВЫЕ ЗАДАНИЯ
Выберите один или несколько правильных ответов
1. В ОСНОВЕ ГЖХ ЛЕЖИТ
1) различие коэффициентов распределения разделяемых веществ между неподвижной жидкой и подвижной газовой фазами
2) распределение смеси веществ на колонке с сорбентом по отдельным зонам в результате повторения актов сорбции и десорбции при пропускании через колонку газа-носителя
3) сорбция газа-носителя на твёрдом сорбенте колонки
4) обратимая хемосорбция ионов анализируемого раствора
2. ОСНОВНЫМИ УЗЛАМИ ГАЗОВОГО ХРОМАТОГРАФА ЯВЛЯЮТСЯ
1) баллон со сжатым газом
2) испаритель
3) хроматографическая колонка
4) детектор
3. В КАЧЕСТВЕ ГАЗА-НОСИТЕЛЯ ИСПОЛЬЗУЮТ
1) водород
2) кислород
3) гелий
4) азот
4. РАЗЛИЧАЮТ СЛЕДУЮЩИЕ ВИДЫ КОЛОНОК
1) насадочная
2) микронасадочная
3) ротационная
4) капиллярная
5. В КАЧЕСТВЕ ТВЁРДЫХ СОРБЕНТТОВ ПРИМЕНЯЮТ
1) диатомит
2) кизельгур
3) кварц
4) крахмал
6. В КАЧЕСТВЕ НЕПОДВИЖНОЙ ЖИДКОЙ ФАЗЫ ИСПОЛЬЗУЮТ
1) вазелиновое масло
2) сложные эфиры
3) силоксановые полимеры с привитыми функциональными группами
4) воду
7. В ГЖХ ХАРАКТЕРЕН ТЕМПЕРАТУРНЫЙ РЕЖИМ
1) комнатная температура
2) изотермический
3) программирование температуры
4) не выше 15 0C
8. ДЕТЕКТОР ХРОМАТОГРАФА ПРЕДНАЗНАЧЕН
1) для обнаружения изменений в составе газа, прошедшего через колонку
2) для разделения веществ
3) для идентификации соединений
4) для обнаружения состава жидкой фазы в хроматографической колонке
9. ДЛЯ АНАЛИЗА ВЕЩЕСТВ ИСПОЛЬЗУЮТ ДЕТЕКТОРЫ
1) по теплопроводности
2) пламенно-ионизационный
3) электронно-захватный
4) рефрактометрический
10. С ГАЗОМ-НОСИТЕЛЕМ АНАЛИЗИРУЕМЫЕ ВЕЩЕСТВА СМЕШИВАЮТСЯ В СОСТОЯНИИ
1) газообразном
2) жидком
3) твёрдом
11. ГЖХ ИСПОЛЬЗУЮТ В ФАРМАЦЕВТИЧЕСКОМ АНАЛИЗЕ ДЛЯ ЦЕЛЕЙ
1) идентификации веществ
2) обнаружения примесей
3) количественного определения компонентов сложных смесей
4) определения биологической активности веществ
12. КАЧЕСТВЕННЫЙ АНАЛИЗ ПРОВОДИТСЯ МЕТОДОМ
1) приведенных удерживаний (объёмное время)
2) введения веществ-свидетелей
3) методом обнаружения химическими реактивами
4 относительных времен удерживания
13. ХАРАКТЕРИСТИКА ВРЕМЕНИ УДЕРЖИВАНИЯ
1) время от момента ввода пробы в хроматографическую колонку до момента выхода из неё максимальной концентрации определяемого вещества
2) время от момента ввода пробы в хроматографическую колонку до момента выхода последнего компонента
3) время от момента ввода пробы до момента выхода растворителя
4) время окончания работы хроматографа
14. КОЛИЧЕСТВЕННЫЙ АНАЛИЗ МЕТОДОМ ГЖХ ПОЗВОЛЯЕТ
1) определить содержание одного, нескольких или всех компонентов в многокомпонентной смеси
2) определить суммарное содержание нескольких компонентов,
объединённых каким-либо общим признаком
3) определить микропримеси в индивидуальных химических соединениях
4) определить содержание лабильных соединений
15. ПАРАМЕТРОМ ХРОМАТОГРАММЫ, ХАРАКТЕРИЗУЮЩИМ КОЛИЧЕСТВО АНАЛИЗИРУЕМОГО КОМПОНЕНТА, ЯВЛЯЕТСЯ
1) площадь пика
2) высота пика
3) произведение высоты пика на время удерживания
4) полуширина пика
16. ОСНОВНЫМИ МЕТОДАМИ КОЛИЧЕСТВЕННОГО АНАЛИЗА СЛУЖАТ
1) метод установления подвижности веществ
2) метод абсолютной градуировки
3) метод внутренней нормализации
4) метод внутреннего стандарта
17. К ПРЕИМУЩЕСТВАМ ГЖХ ОТНОСИТСЯ
1) высокая чувствительность
2) точность
3) возможность анализа термически неустойчивых соединений
4) селективность
ГЛАВА 5
ЖИДКОСТНАЯ ХРОМАТОГРАФИЯ
В жидкостной хроматографии характер протекающих процессов в хроматографической колонке в общем случае идентичен с процессами в ГХ. Отличие состоит в применении в качестве подвижной фазы жидкости, т.е. жидкостная хроматография – это метод разделения смесей веществ в потоке жидкости на поверхности твердого вещества. Подвижной фазой (ПФ) является жидкость, а неподвижной фазой (НФ) является либо тонко измельченная твердая основа, либо жидкость, нанесенная на твердую подложку, либо твердый носитель, химически модифицированный путем введения органических групп.
В связи с высокой плотностью жидких ПФ и большим сопротивлением колонок ЖХ сильно отличается по аппаратурному оформлению от ГХ.
Позже, благодаря широкому изучению процессов кинетики и термодинамики разделения веществ, созданию оборудования, позволяющего осуществить непрерывный и автоматизированный контроль, появляется разновидность жидкостной хроматографии – высокоэффективная хроматография (ВЭЖХ).
ВЫСОКОЭФФЕКТИВНАЯ ЖИДКОСТНАЯ ХРОМАТОГРАФИЯ
(жидкостная хроматография высокого давления)
Современная высокоэффективная жидкостная хроматография высокого давления, скоростная жидкостная хроматография начала развиваться в начале 70-х годов XX века. Разработка нового метода обусловливалась следующими обстоятельствами:
· необходимостью анализа высококипящих (>2000С) или неустойчивых соединений, которые не разделяются методом газовой хроматографии;
· необходимостью увеличения скорости разделения и повышения эффективности метода колоночной жидкостной хроматографии.
ВЭЖХ в настоящее время не только в значительной степени вытеснила классические КХ, ТСХ, БХ, но и обогнала по темпам развития ГХ. Это обусловлено рядом присущих ей преимуществ.
Преимущества ВЭЖХ:
1. Возможность исследования практически любых объектов без каких-либо ограничений по их физико-химическим свойствам.
2. Большой диапазон молекулярных масс веществ, с которыми можно работать.
3. Мягкость условий ВЭЖХ, когда разделение можно проводить при температурах, близких к комнатной.
4. Высокая эффективность.
5. Экспрессность анализа: обычно разделение сложной смеси в ВЭЖХ занимает несколько минут.
6. Высокая чувствительность.
7. Возможность автоматизации разделения и анализа сложных смесей органических и неорганических веществ. В настоящее время в лабораториях имеются полностью автоматизированные хроматографы, которые дают возможность не только автоматически дозировать и проводить хроматографическое разделение целой серии образцов, но и оценивать хроматограммы с помощью предварительной градуировки.
ВЭЖХ представляет хорошо оформленный инструментальный метод, который широко применяют в различных областях науки и техники: биохимия, молекулярная биология, фитохимия, контроль загрязнения окружающей среды, а также в химической, нефтехимической, пищевой и фармацевтической промышленности.
ВЭЖХ – серийный метод определения органических соединений многих классов; его широко используют при анализе смесей аминокислот, белков, различных лекарственных средств с целью установления их подлинности, чистоты и количественного содержания.
Высокоэффективная жидкостная хроматография выполняется под повышенным давлением жидкости до 666,5 кПа (500 атм.).
Разделение смеси происходит в колонке, заполненной сорбентом с очень малым размером зерен (3-5 мкм), и это является основной особенностью ВЭЖХ, поскольку обеспечивает быстрый перенос при высокой эффективности разделения.
Важной особенностью ВЭЖХ (в отличие от ГЖХ) является возможность проведения процесса при комнатной температуре, что ценно при исследовании белков, аминокислот и других неустойчивых соединений.
Разделение смеси достигается за счет различия в сродстве компонентов смеси к неподвижной и подвижной фазам. Основными требованиями в методе является растворимость исследуемых веществ в подвижной фазе (ПФ), а также свойство удерживаться неподвижной фазой (НФ).
|
Просмотров 1950 |
|
|
