
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Физические и химические свойства
|
|
Сульфаниламиды представляют собой белые или белые с желтоватым оттенком кристаллические вещества без запаха. Исключением является салазопиридазин — оранжевого цвета (табл. 43.2).
43.2. Свойства сульфаниламидов
| Лекарственное вещество | Химическая структура | Описание |
| Алифатические (R) производные | ||
| Sulfanilamide— сульфаниламид (Cтрептоцид) |  n-аминобензолсульфамид
n-аминобензолсульфамид
| Белый кристаллический порошок без запаха. Т. пл. 164–167°C |
| Sulfacetamide Sodium— сульфацетамид натрия (Сульфацил-натрий) |  n-аминобензолсульфонилацетамид-натрий моногидрат
n-аминобензолсульфонилацетамид-натрий моногидрат
| Белый кристаллический порошок без запаха |
| Гетероциклические (R) производные | ||
| Sulfadimethoxine— сульфадиметоксин | 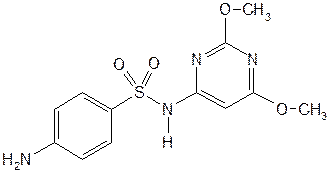 6-(n-аминобензолсульфамидо)-2,4-диметоксипиримидин
6-(n-аминобензолсульфамидо)-2,4-диметоксипиримидин
| Белый или белый с кремоватым оттенком кристаллический порошок без запаха. Т. пл. 198–204°C |
| Sulfalene— сульфален |  2-(n-аминобензолсульфамидо)-3-метоксипиразин
2-(n-аминобензолсульфамидо)-3-метоксипиразин
| Белый или белый с желтоватым оттенком кристаллический порошок без запаха. Т. пл. 174–177°C |
| Ароматические (R1) и гетероциклические (R) производные | ||
| Phtalylsulfathiazole— фталилсульфатиазол (Фталазол) |  2-(n-фталиламинобензолсульфамидо)-тиазол
2-(n-фталиламинобензолсульфамидо)-тиазол
| Белый или белый со слегка желтоватым оттенком порошок |
| Salazodine— салазодин (Салазопиридазин) |  5-(n-[N-(3-метоксипиридазинил-6)-сульфамидо]-фенилазо)-салициловая кислота
5-(n-[N-(3-метоксипиридазинил-6)-сульфамидо]-фенилазо)-салициловая кислота
| Порошок оранжевого цвета без запаха. Т. пл. 202–210°C (с разложением) |
Сульфаниламиды мало растворимы или практически нерастворимы в воде и в таких органических растворителях, как этанол, эфир, хлороформ. Сульфаниламид умеренно растворим в этаноле, а салазодин легко растворим в диметилформамиде. В ацетоне некоторые из них растворимы (сульфаниламид).
Натриевые соли сульфаниламидов (сульфацетамид натрия) легко растворимы в воде и метаноле (при комнатной температуре) и практически нерастворимы или мало растворимы в других органических растворителях (этаноле, эфире, хлороформе, ацетоне).
Растворимость в кислотах и растворах щелочей обусловлена амфотерными свойствами большинства сульфаниламидов. Они проявляют основные свойства, так как в молекуле имеется ароматическая аминогруппа. Поэтому сульфаниламиды, как правило, могут растворяться в кислотах с образованием солей (сильно гидролизованных в растворах):

В разведенных кислотах при комнатной температуре нерастворимы фталилсульфатиазол и салазодин, в молекулах которых атом водорода первичной аминогруппы замещен ароматическим радикалом.
Кислотные свойства у сульфаниламидов выражены сильнее, чем основные. Они обусловлены наличием в молекуле группы –SO2–NH–, содержащей подвижный атом водорода. Вследствие этого сульфаниламиды образуют с щелочами соли:

Поэтому все они легко растворяются в растворах щелочей.
Испытания на подлинность
Для испытаний подлинности сульфаниламидов используют общие и частные реакции, обусловленные наличием тех или иных функциональных групп в молекулах.
Реакция образования азокрасителя. Это общая реакция не только на сульфаниламиды, но и на все соединения, содержащие в молекуле незамещенную первичную ароматическую аминогруппу. Сульфаниламиды, у которых аминогруппа замещена радикалом (фталилсульфатиазол), предварительно гидролизуют кипячением с разведенной хлороводородной кислотой. Реакция основана на образовании хлорида диазония в результате действия раствором нитрита натрия и разведенной хлороводородной кислотой. Последующее сочетание хлорида диазония в щелочной среде с фенолами приводит к образованию азокрасителя. Известно очень большое число азосоставляющих. ГФ рекомендует для выполнения этой реакции щелочной раствор b-нафтола:

В результате реакции появляется вишнево-красное окрашивание или образуется осадок оранжево-красного цвета. В качестве азосоставляющих может использоваться также a-нафтол (тёмно-фиолетовый азокраситель), хинозол (оранжевый). Азокрасители образуются также при взаимодействии с солями диазония ароматических аминов, например, N-(1-нафтил)-этилендиамина. В этом случае азосочетание следует выполнять в слабокислой среде (в сильнокислой среде реакция не идет). Описаны способы идентификации, основанные на использовании роданинов для азосочетания с солями диазония сульфаниламидов (красное окрашивание).
Реакции конденсации. Как и производные n-аминобензойной кислоты, сульфаниламиды образуют в щелочной среде продукты конденсации с 2,4-динитрохлорбензолом (желтого цвета) и в кислой среде окрашенные продукты конденсации с альдегидами типа шиффовых оснований. В качестве реактивов используют n-диметиламинобензальдегид (желтое или оранжевое окрашивание), ванилин (желтое), формальдегид (желто-оранжевое или розовое), уксуснокислый раствор фурфурола (красное или малиново-красное).
Лигниновая проба. Своеобразной разновидностью реакции образования шиффовых оснований является лигниновая проба, используемая для экспресс-анализа. Она выполняется на древесине или газетной бумаге, при нанесении на которую сульфаниламида (или другого первичного ароматического амина) и капли разведенной хлороводородной кислоты появляется оранжево-желтое окрашивание. Сущность происходящего химического процесса в том, что из лигнина образуются ароматические альдегиды: n-оксибензальдегид, сиреневый альдегид, ванилин (в зависимости от вида лигнина). Альдегиды взаимодействуют с первичными ароматическими аминами, образуя шиффовы основания:

Реакции галогенирования. Эти реакции основаны на наличии донорной группы в ароматическом ядре молекулы сульфаниламида (заместитель первого рода):

Реакции галогенирования могут быть использованы как для качественного анализа (образование осадков дибром- или дииодпроизводных), так и для количественного (броматометрического, иодометрического, иодхлорометрического) определения сульфаниламидов.
Реакция обнаружения серы. Наличие серы в молекуле сульфаниламидов, как и в других содержащих серу соединениях, можно установить после окисления органической части молекулы концентрированной азотной кислотой или сплавления с 10-кратным количеством нитрата калия до сульфат-иона. Последний затем обнаруживают с помощью раствора хлорида бария.
Пиролиз сульфаниламидов. При термическом разложении сульфаниламидов в сухой пробирке плавы приобретают различную окраску. Одновременно образуются газообразные продукты. Эта реакция позволяет отличать некоторые сульфаниламиды друг от друга. Так, при пиролизе сульфаниламида (стрептоцида) образуется плав фиолетового цвета и появляется запах аммиака и анилина.
Реакция с растворами солей тяжелых металлов. Ряд ионов тяжелых металлов (меди, кобальта, железа, серебра и др.), замещая подвижный атом водорода сульфамидной группы, образуют с сульфаниламидами внутрикомплексные соединения. Нерастворимые комплексы меди (II) и кобальта (II) имеют различную окраску. Реакции следует выполнять в нейтральной среде, чтобы не допустить образования осадков гидроксидов указанных катионов.
Некоторые из этих цветных реакций могут быть использованы для отличия сульфаниламидов друг от друга. ФС рекомендует использовать реакцию с раствором хлорида кобальта при испытании на подлинность сульфадиметоксина. Образуется ярко-розовый с лиловым оттенком аморфный осадок. Сульфаниламид в этих условиях образует голубоватый с синеватым оттенком осадок, а сульфален приобретает голубое окрашивание. Раствор сульфата меди образует с сульфаниламидом (стрептоцидом) зеленоватый с голубым оттенком осадок, с сульфацетамидом натрия — голубовато-зелёный осадок (не изменяющийся при стоянии), с сульфадиметоксином, сульфаленом и салазодином — зелёного цвета осадки.
Были исследованы методом УФ-спектрофотометрии оптические характеристики продуктов взаимодействия некоторых сульфаниламидов с сульфатом меди (I) в присутствии гидроксиламина (Угрюмова Т. А.). Установлено, в частности, что сульфадиметоксин и салазодин имеют по три максимума поглощения (при 210, 245, 327 нм и 211, 255, 360 нм соответственно). Эти константы предлагаются для идентификации указанных лекарственных веществ. Анализ УФ-спектров поглощения образующихся окрашенных соединений позволил отнести происходящие взаимодействия к реакциям комплексообразования и предположить их химизм, в частности, для сульфадиметоксина:
2CuSO4 + 2NH2OH ¾® Cu2SO4 + N2 + H2SO4 + 2H2O

Разработаны условия использования этой реакции для фотометрического определения, а также применения сульфата меди (II) в присутствии гидроксиламина гидрохлорида для титриметрического определения, в т.ч. в присутствии продуктов гидролиза сульфаниламидов.
Реакция с нитропруссидом натрия. Растворы сульфаниламидов в присутствии едких щелочей при добавлении 1%-ного раствора нитропруссида натрия и последующего подкисления минеральной кислотой образуют окрашенные в красный или красно-коричневый цвет раствор или осадок). Если заменить минеральную кислоту ледяной уксусной, то сульфадиметоксин образует телесного цвета, а сульфален — тёмно-бежевый раствор.
Реакции окисления. Сульфаниламиды, как и другие ароматические амины, довольно легко окисляются. Установлено, что при этом образуются окрашенные соединения хиноидной структуры типа индофенолов. Это используется для идентификации сульфаниламидов. После их извлечения кипящей водой добавляют 3%-ный раствор пероксида водорода и 5%-ный раствор хлорида железа (III). Сульфаниламид в этих условиях приобретает коричнево-красное окрашивание, а затем выпадает осадок желто-бурого цвета. Другие сульфаниламиды также образуют окрашенные растворы и осадки. Если использовать в качестве окислителя хлорамин, то в щелочной среде при сочетании с фенолом образуются индофеноловые красители. Сульфаниламид, в частности, образует краситель синего цвета.
Частные реакции на сульфаниламиды. К числу таких реакций следует отнести обнаружение (по запаху) уксусной кислоты при кислотном гидролизе сульфацетамида натрия; выделение при гидролизе фталилсульфатиазола фталевой кислоты, которую затем идентифицируют по реакции образования флуоресцеина. Для отличия натриевых солей от соответствующих сульфаниламидов выполняют реакцию на ион натрия (окраска бесцветного пламени горелки в желтый цвет).
Сульфацетамид натрия при действии уксусной кислотой выделяет белый осадок сульфацетамида, который после высушивания должен иметь температуру плавления около 183°C:
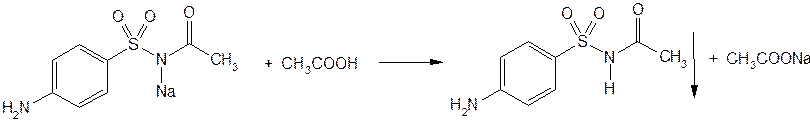
При растворении осадка в этаноле и добавлении концентрированной серной кислоты образуется этилацетат, имеющий характерный запах:

Фталилсульфатиазол при сплавлении с резорцином и каплей концентрированной серной кислоты приобретает оранжево-красное окрашивание. После охлаждения и добавления 2 мл раствора гидроксида натрия отбирают 1 каплю полученной смеси и прибавляют к 200 мл воды. Появляется желтая окраска с интенсивной зеленой флуоресценцией.
Наличие азогруппы в молекуле салазодина подтверждают реакцией гидрирования. Для этого к раствору салазодина прибавляют цинковую пыль и концентрированную хлороводородную кислоту. Окраска раствора постепенно обесцвечивается.
Испытания на чистоту
В сульфаниламидах определяют отсутствие или предельное содержание допустимых количеств органических примесей, сульфатов, хлоридов, сульфатной золы и тяжелых металлов, контролируют pH среды (кислотность или щелочность), прозрачность, цветность растворов. Гидраты (сульфацетамид натрия), сульфаниламид, фталилсульфатиазол и салазодин подвергают проверке на потерю в массе при высушивании. Некоторые сульфаниламиды контролируют на содержание исходных продуктов синтеза. Так, по ФС во фталилсульфатиазоле определяют содержание примеси фталевой кислоты и норсульфазола. Определение этих примесей осуществляют титриметрическими методами. Фталевую кислоту титруют 0,1 М раствором гидроксида натрия в водном извлечении. Примесь норсульфазола (не более 0,5%) определяют нитритометрическим методом.
Для испытания на посторонние органические примеси в сульфалене и сульфадиметоксине используют ТСХ на пластинках Силуфол или Армсорб УФ-254. После хроматографирования в условиях, приведенных в ФС, должно просматриваться только одно пятно, соответствующее стандартному образцу свидетеля. Этот же метод применяют для установления степени чистоты салазодина и определения в нем допустимых количеств примесей салициловой кислоты (2%) и сульфапиридазина (0,5%). Содержание примесей определяют по величине и интенсивности пятен соответствующих свидетелей, нанесенных на ту же пластинку. Аналогичным методом устанавливают наличие посторонних примесей в сульфаниламиде и сульфацетамиде натрия. Устанавливают также микробиологическую чистоту сульфаниламидов (ГФ XI, в. 2, с. 193).
|
Просмотров 7850 |
|
|
