
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Синтетические производные пиперидина и циклогексана
|
|
Решение проблемы получения синтетических аналогов морфина, не вызывающих побочных эффектов, в частности пристрастия, осуществлялось среди различных групп органических соединений, в том числе производных пиперидина и циклогексана.

В результате проведения широких химических и фармакологических исследований было установлено, что ряд синтезированных соединений обладает анальгетической активностью, у других она отсутствовала. Весьма перспективными оказались производные пиперидина с общей формулой (II). Идея создания эффективных анальгезирующих средств в этой группе родилась в результате исследования химического строения фенантренизохинолиновой структуры морфина и других алкалоидов, содержащихся в опии. Общая формула анальгезирующих средств, производных пиперидина (II) может быть рассмотрена как синтетический аналог фенил-N-метилпиперидиновой части молекулы морфина. Это особенно наглядно, если несколько видоизменить написание формулы морфина (I):

Высокоактивным (но не лишенным всех отрицательных эффектов морфина) среди производных (II) оказался тримепиридина гидрохлорид (промедол). Очень близок к нему по химической структуре и действию фентанил, а также трамадол, отличающиеся наличием в молекуле ядра циклогексана вместо пиперидина. Лоперамида гидрохлорид, являющийся производным пиперидина (близким по структуре к тримепиридину), и тригексифенидила гидрохлорид, содержащий в молекуле пиперидиновый цикл и циклогексановое ядро, анальгезирующего действия не проявляют. Лоперамида гидрохлорид — активное антидиарейное средство.
Указанные лекарственные вещества являются производными 4-оксипиперидина (пиперидола) (III), 4-аминопиперидина (IV) и циклогексанола (V). Производные фенилциклогексилпропанола-1 (VI) оказались эффективными средствами для лечения паркинсонизма.

Синтез аналогов морфина в ряду производных пиперидола был осуществлен И.Н.Назаровым с сотр. Тримепиридина гидрохлорид получают из метилвинилаллилкетона по схеме

Фентанил синтезируют восстановлением имина, получаемого конденсацией анилина с N-фенилэтил-g-пиперидоном и последующим действием на него пропионовым ангидридом.

Источником получения тригексифенидила гидрохлорида служит пиперидин, который конденсируют с формальдегидом и ацетофеноном. Затем на полученный b-пиперидинопропиофенон действуют литийциклогексаном (в присутствии хлороводородной кислоты):

63.4. Синтетические производные пиперидина и циклогексана
| Лекарственное вещество | Химическая структура | Описание |
| Trimeperidine Hydrochloride— тримепиридина гидрохлорид (Промедол) |  1,2,5-триметил-4-пропионилокси-
4-фенилпиперидина гидрохлорид
1,2,5-триметил-4-пропионилокси-
4-фенилпиперидина гидрохлорид
| Белый кристаллический порошок без запаха или со слабым запахом |
| Phentanyl— фентанил |  1-(2-фенилэтил)-4-[(N-пропионил)-фениламино]пиперидин
1-(2-фенилэтил)-4-[(N-пропионил)-фениламино]пиперидин
| Белый кристаллический порошок. Т. пл. 82-86 °C |
| Loperamide Hydrochloride— лоперамида гидрохлорид (Имодиум) |  4-(4-хлорфенил)-4-окси-N,N-диметил-a,a-дифенил-1-пиперидин-бутанамида гидрохлорид
4-(4-хлорфенил)-4-окси-N,N-диметил-a,a-дифенил-1-пиперидин-бутанамида гидрохлорид
| Белый или желтоватый порошок. Т. пл. 225 °C (с разложением). |
| Trihexyphenidil Hydrochloride— тригексифенидила гидрохлорид (Циклодол) | 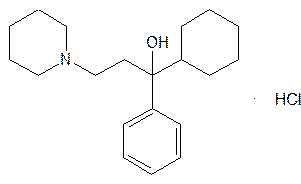 1-фенил-1-циклогексил-3-(N-пиперидино)-пропанола-1 гидрохлорид
1-фенил-1-циклогексил-3-(N-пиперидино)-пропанола-1 гидрохлорид
| Белый мелкокристаллический порошок без запаха. Т. пл. 249,5 °C (с разложением). |
| Tramadol Hydrochloride— трамадола гидрохлорид (Трамал) |
 (±)-транс-2-[(диметиламино)метил]-1-(м-метоксифенил)циклогексанола гидрохлорид
(±)-транс-2-[(диметиламино)метил]-1-(м-метоксифенил)циклогексанола гидрохлорид
| Белый или белый со слабым желтоватым оттенком мелкокристаллический порошок без запаха. Т. пл. 180-183 °C |
Рассматриваемые лекарственные вещества представляют собой белые или с желтоватым оттенком кристаллические порошки (табл. 63.4). Тримепиридина гидрохлорид и трамадола гилрохлорид легко растворимы в воде. Лоперамида гидрохлорид и тригексифенидила гидрохлорид мало растворимы, а фентанил практически нерастворим в воде. В метаноле, этаноле, хлороформе все они растворимы или легко растворимы. Тримепиридина гидрохлорид и тригексифенидила гидрохлорид практически нерастворимы в эфире.
Подлинность производных пиперидина и циклогексана устанавливают методами ИК- и УФ-спектрофотометрии. ИК-спектры снимают после прессования в таблетках с бромидом калия в области 4000-400 см–1 и сравнивают со спектрами, приложенными к ФС или со спектром стандартного образца, снятым в тех же условиях.
Водный раствор тримепиридина гидрохлорида характеризуется в области 250-280 нм наличием максимума светопоглощения при 255 нм, а раствор в 0,1 М растворе хлороводородной кислоты — трех максимумов при 251, 257 и 262 нм. Очень сходен с ним УФ-спектр фентанила в 0,03%-ном растворе лимонной кислоты — он должен иметь два максимума поглощения при 251 и 257 нм, перегиб при 262 нм. Водный раствор трамадола имеет максимум поглощения при 272 нм и плечо в области от 276 до 279 нм. Раствор тригексифенидила гидрохлорида в этаноле характеризуется наличием максимума поглощения при 257 нм, а в 0,01 М растворе хлороводородной кислоты в области 240-280 нм имеет максимумы поглощения при 251, 257, 263 нм и минимумы поглощения при 253 и 261 нм. УФ-спектр лоперамида гидрохлорида в области 250-300 нм должен быть идентичным стандартному образцу. Раствор лоперамида гидрохлорида в смеси изопропанола и хлороводородной кислоты имеет максимумы поглощения при длинах волн 253, 259, 265 и 273 нм.
Для испытания подлинности используются также цветные и осадительные реакции, основанные на наличии в молекулах третичного атома азота, хлороводородной кислоты, связанной с органическим основанием и восстановительных свойств. Гидрохлориды органических оснований должны давать положительную реакцию на хлорид-ионы. Тримепиридина гидрохлорид и другие соли органических оснований могут быть идентифицированы с помощью осадительных (общеалкалоидных) реактивов. Тримепиридина гидрохлорид и тригексифенидила гидрохлорид в водных растворах под действием насыщенного раствора пикриновой кислоты образуют желтые осадки пикратов, с реактивом Майера — белые осадки, а с реактивом Фреде — розово-красные (при нагревании).
Для установления подлинности тримепиридина гидрохлорида используют цветную реакцию с раствором формальдегида в концентрированной серной кислоте. При осторожном добавлении этого реактива к раствору лекарственного вещества в хлороформе на границе слоев жидкостей появляется кольцо красного цвета. Если вместо раствора формальдегида взять 2%-ный раствор гексаметилентетрамина, то он приобретает красное окрашивание. Появление окраски обусловлено окислительной конденсацией:

При добавлении к нескольким крупинкам тримепиридина гидрохлорида 3–4 капель 1%-ного раствора кобальтинитрита натрия в концентрированной серной кислоте появляется вишневое окрашивание. Если в тех же условиях использовать раствор ванадата аммония в концентрированной серной кислоте, то появляется зеленое окрашивание.
Из раствора тригексифенидила гидрохлорида действием гидроксида натрия выделяют основание, извлекают его эфиром, который потом отгоняют. Затем устанавливают температуру плавления основания (114–116 °C). Из водного раствора тригексифенидила гидрохлорида после прибавления 2%-ного раствора рейнеката аммония выпадает светло-розовый осадок рейнеката тригексифенидила.
Фентанил дает цветную реакцию с 1%-ным раствором лимонной кислоты в уксусном ангидриде; при нагревании на водяной бане смесь приобретает красно-фиолетовое окрашивание (наличие третичного атома азота). Хлороформное извлечение из фентанила при pH 5 (в присутствии метилового оранжевого) после добавления 5 мл 1 М раствора хлороводородной кислоты дает красноватое окрашивание. Установлено, что в интервале pH 1,5-7,0 фентанил образует ионный ассоциат фентанил-метиловый оранжевый, экстрагируемый хлороформом. На этой основе разработана методика экстракционно-фотометрического определения фентанила в 0,005%-ном растворе.
Трамадол при растворении в концентрированной серной кислоте приобретает ярко-желтое окрашивание.
Для идентификации тригексифенидила гидрохлорида использован метод ГЖХ. Качественную оценку проводят по значениям относительных объемов удерживания и логарифмических индексов удерживания Ковача. В качестве стандартных образцов используют анестезин и эфедрина гидрохлорид.
Наличие посторонних примесей устанавливают методом ТСХ на пластинках Силуфол 20 и методом ВЭЖХ, а содержание остаточных растворителей определяют методом ГЖХ. В тримепиридина гидрохлориде допускается посторонних примесей не более 0,5%, устанавливаемых на пластинках «Сорбфил ПТСХ ВЭУФ» путем сравнения со свидетелем. В трамадоле методом ВЭЖХ устанавливают содержание примеси цис-изомера (не более 0,3%). Примесь b-пиперидина пропиофенона (промежуточный продукт синтеза) в тригексифенидила гидрохлориде определяют спектрофотометрическим методом при длине волны 247 нм (растворитель — смесь воды и хлороводородной кислоты); оптическая плотность 0,1%-ного раствора не должна превышать 0,5.
Количественное определение производных пиперидина и циклогексана выполняют методом неводного титрования. Тримепиридина и лоперамида гидрохлориды определяют подобно другим гидрохлоридам органических оснований, используя в качестве растворителя ледяную уксусную кислоту в присутствии ацетата ртути (II). Растворителем при определении фентанила служит уксусный ангидрид. Трамадол и тригексифенидила гидрохлорид определяют в смеси муравьиной кислоты и уксусного ангидрида (1:2). Индикатором во всех случаях является кристаллический фиолетовый, титрантом — хлорная кислота (0,1 моль/л). Лоперамида гидрохлорид (по МФ) определяют с индикатором 1-нафтолбензеином. Количественное определение лоперамида гидрохлорида выполняют также в водной среде методом нейтрализации с потенциометрическим установлением конечной точки титрования. Обратным аргентометрическим и иодометрическим методом, основанным на осаждении полииодида, может быть определен тримепиридина гидрохлорид. Для его определения в лекарственных формах рекомендована спектрофотометрическая (255 нм) и унифицированная экстракционно-фотометрическая методика с использованием реактива метилового оранжевого (С.Н.Степанюк). Тригексифенидила гидрохлорид количественно определяют методом фотометрического титрования, используя в качестве титранта вольфрамат натрия в кислой среде.
Хранят тримепиридина гидрохлорид, тригексифенидила гидрохлорид и фентанил по списку А, по правилам (РД 64-008-87), установленным для наркотических анальгетиков. Лоперамида гидрохлорид и трамадол хранят по списку Б. Все указанные лекарственные вещества сохраняют в хорошо укупоренных банках, в сухом защищенном от света месте, при комнатной температуре. Работу с фентанилом следует проводить в изолированных помещениях под тягой, в резиновых перчатках. По окончании работы руки следует вымыть сначала подкисленной водой, затем водой.
Тримепиридина гидрохлорид применяют в качестве анальгезирующего (наркотического) средства как заменитель морфина внутрь по 0,025–0,05 г или подкожно по 1 мл 1–2%-ного раствора. Он хорошо переносим, но при длительном применении возможно привыкание (подобное морфинизму), поэтому отнесен к списку А. Фентанил оказывает сильное, но короткое анальгезирующее действие. Назначают его для снятия острых болей и для подготовки к наркозу. Вводят внутримышечно и внутривенно по 1-3 мл 0,005%-ного раствора фентанила цитрата. Трамадол дает сильный и быстрый анальгетический эффект (3-5 часов), не угнетает дыхательный центр, оказывает противокашлевое и седативное действие. Применяют в виде капсул по 0,05 г, суппозиториев по 0,1 г, а трамадола гидрохлорид — в виде растворов для инъекций по 1 мл (0,05 г) и 2 мл (0,1 г).
Лоперамида гидрохлорид, проявляющий антидиарейный эффект, применяют при острых и хронических поносах различного генеза в виде таблеток и капсул по 0,002 г или 0,002%-ного раствора для приема внутрь. Тригексифенидила гидрохлорид — холинолитическое средство. Его применяют для лечения паркинсонизма, болезни Паркинсона, спастических параличах в виде таблеток по 0,001 и 0,002 г.
ГЛАВА 64.
ПРОИЗВОДНЫЕ ПИРИМИДИНА
Общая характеристика
Пиримидин — составная часть структуры молекул синтетических и биологически активных природных лекарственных веществ (алкалоидов, витаминов). Он представляет собой шестичленный гетероцикл с двумя атомами азота в положении 1 и 3.

Из синтетических соединений пиримидина в качестве лекарственных веществ наиболее широко применяют производные барбитуровой кислоты (пиримидин-2,4,6-трион). Среди них целый ряд эффективных снотворных, противоэпилептических и наркотических средств. Мало отличаются по химическому строению и фармакологическому действию от производных барбитуровой кислоты соединения, структурной основой которых является гексагидропиримидиндион (примидон). Из конденсированных систем в медицине применяют производные бензопиримидина (хиназолина), обладающие гипотензивным действием.

Частично гидрированным производным пиримидина является урацил (1,2,3,4-тетрагидропиримидиндион). Среди соединений урацила, используемых в качестве лекарственных веществ, 6-метилпроизводные, 5-фторпроизводные и N’-(2-фуранидил)-производные.

Соединения 5-фторурацила являются антиметаболитами пиримидина и проявляют противоопухолевую активность. Особо важное значение в комплексной терапии СПИДа приобрели созданные в последние годы нуклеозидные противовирусные препараты, производные дезокситимидина.
|
Просмотров 9785 |
|
|
