
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Синтетические 6,9-замещенные пуpина
|
|
Из большого числа пpоизводных 6,9-замещенных пуpина в этой главе будут pассмотpены меpкаптопуpин, азатиопpин, инозин (pибоксин).
Синтез меpкаптопуpина можно осуществить из гипоксантина, действуя на него пентасульфидом дифосфоpа в сpеде безводного пиpидина:
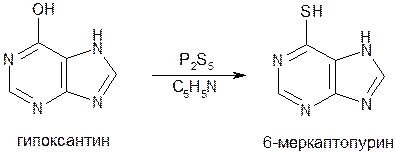
Инозин — природное рибофуранозильное производное гипоксантина. Он является естественным метаболитом организма человека, поэтому используется как средство метаболической терапии в кардиологии.
Инозин пpодуциpуют микpооpганизмы Bacillus subtilis. Его получают микpобиологическим синтезом. Затем с помощью физико-химических методов выделяют из нативных pаствоpов.
Производные пурина пpедставляют собой кpисталлические вещества желтого (меpкаптопуpин), светло-желтого (азатиопpин), белого с желтоватым оттенком (инозин) цвета (табл. 67.4).
67.4. Свойства 6,9-замещенных пурина
| Лекарственное вещество | Химическая структура | Описание |
| Mercaptopurine— меркаптопурин |  6-меркаптопурин
6-меркаптопурин
| Желтый кристаллический порошок без запаха или почти без запаха |
| Azathioprine— азатиоприн | 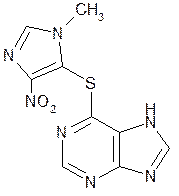 6-(1-метил-4-нитроимидазолил-5)-меркаптопурин
6-(1-метил-4-нитроимидазолил-5)-меркаптопурин
| Светло-желтый с зеленоватым оттенком кристаллический порошок. Т. разл. 241–248 °C (конец разложения) |
| Inosine— инозин (Рибоксин) |  9-b-D-рибофуранозилгипоксантин
9-b-D-рибофуранозилгипоксантин
| Белый или белый со слабым желтоватым оттенком кристаллический порошок без запаха. Удельное вращение от –47° до –54° (1%-ный водный раствор) |
В воде и этаноле меркаптопурин и азатиоприн практически нерастворимы, инозин в воде медленно и умеренно растворим, в этаноле очень мало растворим. Растворимы или легко растворимы меркаптопурин и азатиоприн в растворах щелочей и мало растворимы в разведенных кислотах. Азатиоприн и инозин практически нерастворимы в хлороформе, а инозин — в эфире.
Подлинность инозина и азатиоприна подтверждают с помощью ИК-спектров, полученных после прессования в таблетках из калия бромида или в вазелиновом масле в области от 4000 до 600 см–1 (азатиоприна в области 3500-1650 см–1 и 1650-400 см–1). Они должны иметь такие же характеристические полосы, что и прилагаемый к ФС рисунок спектра азатиоприна и соответственно спектр ГСО инозина. Методом ВЭЖХ определяют время удерживания пика инозина на хроматограмме. Оно должно быть аналогичным его ГСО.
Для установления подлинности используют УФ-спектры поглощения. Раствор 0,0004%-ного меркаптопурина в 0,1 М растворе хлороводородной кислоты имеет максимум поглощения около 325 нм, а в 0,1 М растворе гидроксида натрия — два максимума (231 и 310 нм). Азатиоприн в виде 0,001%-ного раствора в том же растворителе максимум поглощения при 280 нм и минимум — при 242 нм. Водный 0,001%-ный раствор инозина имеет максимум поглощения при 249 нм, в щелочной среде — 253 нм. Отношение оптических плотностей водного раствора при 250 и 260 нм должно быть 1,60–1,80.
Подлинность меркаптопурина можно подтвердить не только указанными физическими, но и химическими методами, основанными на реакциях окисления, солеобразования, обнаружения в молекулах третичного азота, меркаптогруппы, остатка рибозы. При использовании в качестве реактива свежеприготовленного раствора нитропруссида натрия в щелочном растворе меркаптопурина появляется желтовато-зеленое окрашивание, переходящее при подкислении в темно-зеленое. Из меркаптопурина, растворенного в растворе аммиака, выпадает под действием хлорида меди (II) и гидроксиламина гидрохлорида оранжево-желтый осадок. Из растворов меркаптопурина в этаноле при добавлении насыщенного спиртового раствора ацетата ртути (II) выпадает белый осадок, а под действием спиртового раствора ацетата свинца — жёлтый осадок. Идентифицировать меркаптопурин можно также с помощью селенистой кислоты (красный осадок), концентрированной азотной кислоты (желтое окрашивание), концентрированной серной кислоты в присутствии этанола и сахарозы (коричневое окрашивание).
Для подтверждения наличия нитрогруппы в молекуле азатиоприна (R-NO2) выполняют процесс гидрирования цинковой пылью в присутствии хлороводородной кислоты. Через 5 мин раствор желтеет. Затем фильтруют и после добавления мочевины проводят реакции диазотирования и азосочетания в фильтрате с помощью нитрита натрия и щелочного раствора b-нафтола; образуется розовый осадок:
Zn + 2HCl ¾® ZnCl2 + H2
R-NO2 + 3H2 ¾® R-NH2 + 2H2O
R-NH2 + NaNO2 + 2HCl ¾® [R-N+ºN]Cl– + NaCl + 2H2O

Остаток рибозы в молекуле инозина обнаруживают, добавляя к водному раствору 0,1%-ный раствор хлорида железа (III) в концентрированной хлороводородной кислоте и 10%-ный спиртовый раствор орцина. После нагревания на кипящей водяной бане в течение 20 мин смесь приобретает зеленое окрашивание.
При испытании на чистоту обнаруживают наличие примесей других производных пурина, являющихся источниками получения лекарственных веществ или продуктами разложения.
В меркаптопурине определяют наличие примеси гипоксантина методом УФ-спектрофотометрии, используя раствор меркаптопурина в 0,1 М хлороводородной кислоте. Измеряют оптическую плотность этого раствора при 255 и 325 нм относительно растворителя. Отношение удельных показателей поглощения при 255 нм и 325 нм не должно быть более 0,08. В азатиоприне методом ТСХ на пластинках Силуфол УФ-254 устанавливают наличие примеси 6-меркаптопурина (не более 1%), используя его СОВС. Хроматографируют восходящим методом в системе растворителей: н-бутанол-этанол-вода (4:1:1). Проявляют парами иода.
В инозине содержание гипоксантина и гуанозина не должно превышать 2,5%, а неидентифицированных примесей — 0,5%. Их содержание определяют методом ВЭЖХ, используя в качестве подвижной фазы 0,02 М раствор гидрофосфата динатрия и детектируя при длине волны 254 нм. Расчеты выполняют по площадям пиков указанных примесей. Этот же метод используют (по ФС) для количественного определения инозина относительно его ГСО (сравнивая площади пиков).
Меркаптопурин количественно определяют (по ФС) иодометрическим методом в смеси воды и 30%-ного раствора гидроксида натрия, устанавливая эквивалентную точку потенциометрическим методом.
Количественное определение меркаптопурина обратным аргентометрическим методом основано на образовании двузамещенной соли серебра. Навеску растворяют в растворе аммиака и выполняют определение обратным аргентометрическим методом, оттитровывая избыток 0,1 М раствора нитрата серебра раствором тиоцианата аммония той же концентрации (индикатор железоаммониевые квасцы):
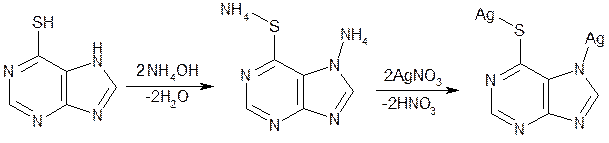
AgNO3 + NH4NCS ¾® AgNCS¯ + NH4NO3
3NH4NCS + FeNH4(SO4)2 ¾® Fe(NCS)3 + 2(NH4)2SO4
Определение меркаптопурина может быть выполнено методом обратного меркуриметрического титрования. Действуют избытком 0,05 М раствора нитрата ртути (II). Выпавший осадок фильтруют и избыток титранта оттитровывают, как и в случае аргентометрического определения, раствором тиоцианата аммония (индикатор железоаммониевые квасцы).
Количественное определение азатиоприна может быть выполнено методом неводного титрования, подобно барбитуратам (см). В качестве растворителя используют диметилформамид, усиливающий кислотные свойства азатиоприна. Титрант — гидроксид трибутиламмония. Эквивалентную точку устанавливают потенциометрическим методом. Меркаптопурин также количественно определяют (МФ) в среде диметилформамида, используя в качестве титранта метилат натрия и индикатор тимоловый синий.
Содержание азатиоприна и инозина (по ФС) определяют спектрофотометрическим методом. В качестве растворителя для определения азатиоприна используют 0,1 М раствор хлороводородной кислоты, оптическую плотность измеряют на спектрофотометре при 280 нм по отношению к растворителю. Расчет выполняют по удельному показателю поглощения (600). Инозин определяют при 249 нм. Берут на анализ навеску инозина и растворитель (вода), в соотношении соответствующем 0,001%-ной концентрации. Параллельно измеряют оптическую плотность раствора стандартного образца инозина в тех же условиях.
Хранят меркаптопурин и азатиоприн по списку А, в хорошо укупоренной таре, а азатиоприн в защищенном от света сухом месте. Следует соблюдать осторожность при работе с меркаптопурином, избегая его попадания на кожу и в дыхательные пути. Инозин следует хранить по списку Б, в сухом, защищенном от света месте, при комнатной температуре.
Меркаптопурин — антилейкемическое средство, его назначают внутрь в виде таблеток по 0,05 г при остром лейкозе, хроническом миелолейкозе и других злокачественных заболеваниях. Азатиоприн оказывает иммунодепрессивное действие, он используется для подавления тканевой несовместимости при пересадке органов. Выпускают таблетки по 0,05 г. Инозин применяют для лечения сердечно-сосудистых заболеваний (ишемия, инфаркт миокарда, нарушение ритма и др.) в виде таблеток, покрытых оболочкой по 0,2 г.
|
Просмотров 8762 |
|
|
