
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Общая характеристика и синтез
|
|
Фенотиазин представляет собой конденсированную гетероциклическую систему, состоящую из шестичленного гетероцикла тиазина и двух ядер бензола:

Производные фенотиазина представляют собой одну из самых важных и перспективных групп лекарственных веществ в современной фармации и фармакологии. История создания первого антипсихотического средства — хлорпромазина начинается с 30-х годов XX века, когда среди производных фенотиазина искали противогистаминные препараты. При этом обнаружилось, что ряд из них проявляет также нейролептическое и антипсихотическое действие, а ацилпроизводные фенотиазина — антиаритмическое действие.
В нашей стране (М.Н.Щукина, А.П.Сколдинов, С.В.Журавлев, Н.В.Савицкая) и за рубежом в 50-х годах было синтезировано большое число производных фенотиазина, имеющих общую формулу:

70.1. Зависимость между химической структурой и действием
производных фенотиазина
| Лекарственное вещество | Заместители | Более выраженное фармакологическое действие | |
| R1 | R2 | ||
| Промазин (Пропазин) |

| – | Нейролептическое |
| Прометазин (Дипразин) |

| – | Противогистаминное (противоаллергическое) |
| Хлорпромазин (Аминазин) |

| –Cl | Нейролептическое |
| Левомепромазин | 
| –OCH3 | « |
| Трифлуоперазин (Трифтазин) | 
| –CF3 | « |
| Морацизин (Этмозин) | 
| 
| Антиаритмическое |
| Этацизин | 
| 
| « |
По химической структуре и характеру выраженного фармакологического действия производные фенотиазина, можно разделить на две группы. К первой из них следует отнести 10-алкилпроизводные фенотиазина: промазин, левомепромазин, прометазин, хлорпромазин, трифлуоперазин, обладающие нейролептическим и противогистаминным действием, а ко второй — 10-ацилпроизводные фенотиазина: морацизин, этацизин, которые эффективны при лечении сердечно-сосудистых заболеваний (табл. 70.1).

Синтез производных фенотиазина состоит из трех стадий: получения фенотиазинового ядра, синтеза алкильного или ацильного радикала, присоединения этого радикала к фенотиазиновому ядру (в положении 10) и получение гидрохлорида органического основания.
Для синтеза хлорпромазина гидрохлорида предварительно получают 2-хлорфенотиазин из 2,4-дихлортолуола:
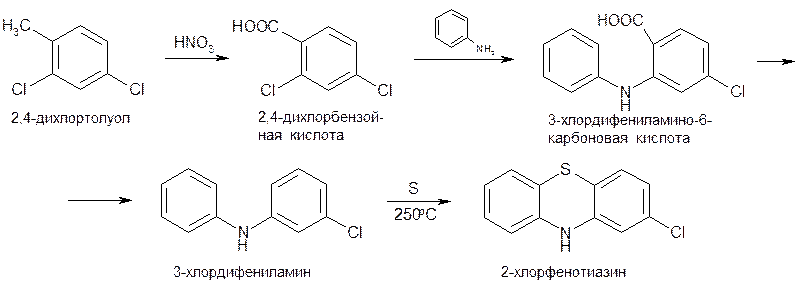
Диалкиламиноалкильные соединения предварительно синтезируют из простых органических веществ. Например, 3-диметиламинопропилхлорид получают по схеме
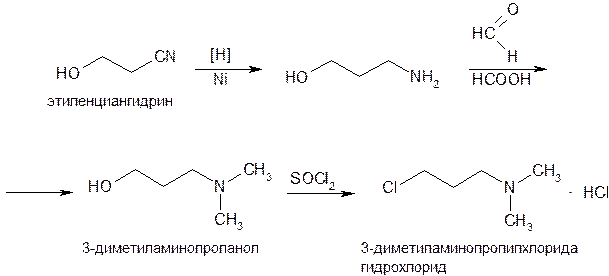
Присоединение диалкиламиноалкилхлоридов к фенотиазиновому ядру осуществляют замещением атома водорода в положении 10. Вначале получают органическое основание, а затем гидрохлорид. Примером может служить третья стадия синтеза хлорпромазина гидрохлорида из 2-хлорфенотиазина и гидрохлорида 3-диметиламинопропилхлорида:
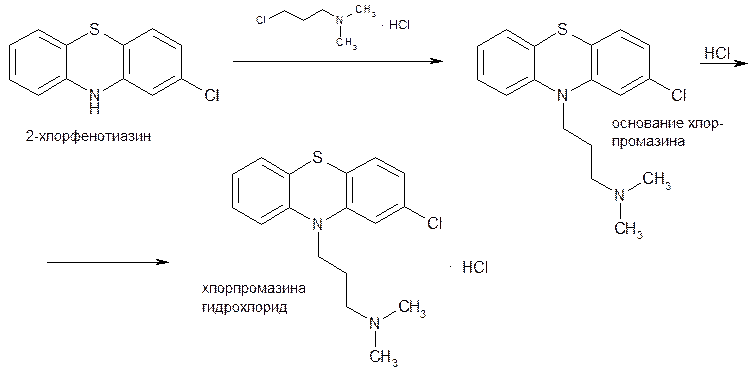
По аналогичным схемам получают и другие 10-алкилпроизводные фенотиазина.
Синтез 10-ацилпроизводных фенотиазина отличается от синтеза 10-алкилпроизводных тем, что на стадии замещения атома водорода в положении 10, действуют не диалкиламиноалкилхлоридом, а хлорангидридом b-хлорпропионовой кислоты:

Затем замещают атом хлора соответствующим радикалом. По этой схеме был осуществлен синтез морацизина, этацизина и др.
По физическим свойствам производные фенотиазина (табл. 70.2) представляют собой белые (или со слабым желтоватым, сероватым, кремовым оттенком) кристаллические вещества. Производные фенотиазина легко окисляются, в том числе и кислородом воздуха. Поэтому на свету они темнеют.
70.2. Свойства производных фенотиазина
| Лекарственное вещество | Химическая структура | Описание |
| 10-алкилпроизводные фенотиазина | ||
| Promazine Hydrochloride— промазина гидрохлорид (Пропазин) |  10-(3’-диметиламинопропил)фенотиазина
гидрохлорид
10-(3’-диметиламинопропил)фенотиазина
гидрохлорид
| Белый или белый со слабым желтоватым оттенком кристаллический порошок без запаха. Гигроскопичен. Т. пл. 177–181°C |
| Promethazine Hydrochloride— прометазина гидрохлорид (Дипразин) |  10-(2’-диметиламинопропил)фенотиазина
гидрохлорид
10-(2’-диметиламинопропил)фенотиазина
гидрохлорид
| Белый кристаллический порошок без запаха. Т. пл. 221–225°C (с разложением) |
| Chlorpromazine Hydrochloride— хлорпромазина гидрохлорид (Аминазин) |  2-хлор-10-(3’-диметиламинопропил)
фенотиазина гидрохлорид
2-хлор-10-(3’-диметиламинопропил)
фенотиазина гидрохлорид
| Белый или белый со слабым кремовым оттенком кристаллический порошок. Гигроскопичен. Т. пл. 195–198°C |
| Levomepromazine— левомепромазин (Тизерцин) |  2-метокси-10-(3’-диметиламино-2’-метилпропил)-фенотиазина гидрохлорид
2-метокси-10-(3’-диметиламино-2’-метилпропил)-фенотиазина гидрохлорид
| Желтовато-белый слегка гигроскопичный порошок. Неустойчив к свету и воздуху |
| Trifluoperazine Hydrochloride— трифлуоперазина гидрохлорид (Трифтазин) |  2-трифторметил-10-[3’-(1’’-метилпиперазинил-4’’)-пропил]-
фенотиазина дигидрохлорид
2-трифторметил-10-[3’-(1’’-метилпиперазинил-4’’)-пропил]-
фенотиазина дигидрохлорид
| Белый или слегка зеленовато-желтоватый кристаллический порошок без запаха. Т. пл. 232–240°C |
| 10-ацилпроизводные фенотиазина | ||
| Moracizine Hydrochloride— морацизина гидрохлорид (Этмозин) |  2-карбэтоксиамино-10-(3’-морфолилпропионил)
фенотиазина гидрохлорид
2-карбэтоксиамино-10-(3’-морфолилпропионил)
фенотиазина гидрохлорид
| Белый или белый с кремовым оттенком кристаллический порошок |
| Ethacizine— этацизин |  2-карбэтоксиамино-10-(3’-диэтиламинопропионил)
фенотиазина гидрохлорид
2-карбэтоксиамино-10-(3’-диэтиламинопропионил)
фенотиазина гидрохлорид
| Белый кристаллический порошок. Т. пл. 199–208°C |
Производные фенотиазина очень легко или легко растворимы в воде, легко растворимы или растворимы в этаноле, практически нерастворимы в эфире. Морацизина гидрохлорид и этацизин отличаются несколько меньшей растворимостью. Морацизина гидрохлорид растворим в воде, умеренно растворим в этаноле. Этацизин медленно растворим в воде, растворим в этаноле. Промазина, прометазина, хлорпромазина гидрохлориды левомепромазин и этацизин легко растворимы в хлороформе.
Способы испытаний
Для испытания подлинности производных фенотиазина используют спектрофотометрию в УФ-области. ФС рекомендует устанавливать удельный показатель поглощения при испытании трифлуоперазина дигидрохлорида (0,001%-ный раствор в 0,01 М растворе хлороводородной кислоты при длине волны 256 нм). УФ-спектр раствора промазина гидрохлорида в 0,01 М растворе хлороводородной кислоты имеет в области 230-380 нм два максимума поглощения — при 252 и 302 нм. УФ-спектр 0,0005%-ного раствора прометазина гидрохлорида в тех же условиях имеет максимумы светопоглощения при 249 и 300 нм, хлорпромазина гидрохлорида — при 254 и 307 нм. Подлинность левомепромазина гидрохлорида устанавливают по идентичности УФ-спектров испытуемого и стандартного растворов.
А.П.Арзамасцевым с сотр. систематизированы сведения о применении УФ- и ИК-спектроскопии для оценки подлинности 12 лекарственных веществ, производных фенотиазина. Установлено, что оптимальный растворитель для УФ-спектроскопии — этанол. УФ-спектры 10-алкилпроизводных фенотиазина имеют по два максимума поглощения в области 290–330 нм; у 10-ацилпроизводных наблюдается гипсохромное смещение обоих максимумов. ИК-спектры, снятые после прессования в таблетках бромида калия на двухлучевом ИК-спектрофотометре в области 4000–250 см–1, насчитывают по 20–25 полос поглощения. Основным отличительным признаком ИК-спектров 10-ацилпроизводных (от 10-алкилпроизводных) служат максимумы поглощения в области 1680–1660 см–1, обусловленные наличием в молекуле амидного карбонила. Другие полосы поглощения, связанные с особенностями химической структуры, позволяют отличать друг от друга производные фенотиазина (ФС).
ВЭЖХ оказалась перспективной для контроля качества лекарственных веществ 10-алкил- и 10-ацилпроизводных фенотиазина. Разработаны четыре варианта селективного разделения 16 производных данной группы, которые можно использовать для их идентификации, контроля чистоты и количественного определения в лекарственных формах (В.И.Прокофьева).
Кроме физико-химических методов для испытания производных фенотиазина применяют химические реакции окисления, соле- и комплексообразования, обнаружения атомов азота, серы, хлорид-иона. В большинстве испытаний подлинности используют способность производных фенотиазина легко окисляться с образованием окрашенных продуктов. Так, при действии 10%-ным раствором хлорамина Т появляется фиолетовая или красно-фиолетовая окраска, переходящая в слой хлороформа. В качестве окислителей могут быть применены бромная вода, азотная кислота, хлорид железа (III), пероксид водорода, концентрированная серная кислота. Реакции эти в большинстве своем мало специфичны, т.к. образуются смеси продуктов окисления, имеющие красное, вишнево-красное, красно-оранжевое, малиновое окрашивание.
Более специфичным из перечисленных реактивов на фенотиазиновое ядро является бромная вода (табл. 70.3). Этот реактив используют (ФС) для отличия производных фенотиазина друг от друга (растворы лекарственных веществ нагревают до кипения с бромной водой).
70.3. Цветные реакции производных фенотиазина с бромной водой
| Лекарственное вещество | Результат реакции |
| Промазина гидрохлорид | Прозрачный буровато-красный раствор |
| Прометазина гидрохлорид | Мутный темно-вишневый раствор со взвешенным осадком |
| Хлорпромазина гидрохлорид | Прозрачный светло-малиновый раствор |
| Трифлуоперазина гидрохлорид | Вначале коричневый, а затем бледно-розовый раствор |
| Морацизина гидрохлорид и этацизин | Вначале светло-сиреневый, а затем ярко-фиолетовый раствор |
Окрашенные продукты, получающиеся при нагревании производных фенотиазина с бромной водой, обусловлены образованием пербромпроизводных катиона фенотиазония. Фенотиазин при окислении бромом образует окрашенный в красный цвет пербромфенотиазоний:

Вместо нестойкого и токсичного реактива — бромной воды был предложен и включен в ФС для испытания подлинности 10-алкилпроизводных фенотиазина (промазина, прометазина, хлорпромазина, трифлуоперазина гидрохлоридов) 1%-ный водный раствор калия бромата в присутствии 0,15 мл разведенной хлороводородной кислоты. Водные или водно-спиртовые 0,1%-ные растворы указанных лекарственных веществ приобретают розовое или розово-оранжевое окрашивание, постепенно переходящее в малиновое или коричневое. В отличие от других из окрашенного раствора прометазина гидрохлорида выпадает осадок вишнево-красного цвета.
Для идентификации 10-ацилпроизводных фенотиазина (морацизина гидрохлорида и этацизина) рекомендовано использовать в качестве реактива 1%-ный раствор калия бромата, но после предварительного гидролиза с разведенной хлороводородной кислотой (при нагревании в течение 15 мин). Последующая методика выполнения такая же, как и для 10-алкилпроизводных фенотиазина. Указанная группа производных фенотиазина образует также окрашенные продукты окисления со щелочным раствором гидроксиламина при рH 4,0. Окраска зависит от характера радикала в положении 2 (В.И.Прокофьева).
Левомепромазин под действием концентрированной серной кислоты приобретает сиреневое окрашивание. Для идентификации производных фенотиазина можно использовать реакцию с концентрированной серной кислотой или с 50–60%-ными растворами этой кислоты в присутствии других окислителей. Для некоторых производных фенотиазина добавляют в реакционную смесь ванадат аммония (реактив Манделина). При добавлении к водному раствору прометазина гидрохлорида порошка оксида свинца в верхнем слое не должно быть красного окрашивания, но он медленно становится синеватым. Образуются и другие продукты окисления, имеющие максимумы поглощения в УФ- и видимой областях спектра. Положительные результаты дают указанные химические реакции при анализе левомепромазина. При добавлении к раствору левомепромазина 1 мл 37%-ного раствора формальдегида и нескольких капель 0,1 М раствора сульфата церия появляется интенсивная лиловая окраска. В основе этих испытаний лежит процесс окисления производных фенотиазина, который в зависимости от химической структуры протекает при нагревании или при комнатной температуре.
Наибольшей реакционной способностью в молекулах производных фенотиазина отличается атом серы, который способен окисляться с образованием различных веществ. Продуктами окисления 10-замещенных фенотиазинов являются парамагнитные катион-радикалы фенотиазония (I), которые при последующем окислении превращаются в диамагнитные ионы феназтиония (II). Последние при взаимодействии с водой образуют сульфоксиды (III), сульфоны и 3-ониевые продукты:

Таким образом, конечными продуктами окисления могут быть 9-S-оксид, 9,9-диоксид (сульфон), 3-окси-, 3,7-диокси, 3-он-, 3-окси-7-он-фенотиазины.
В отличие от других производных фенотиазина с трифлуоперазина гидрохлоридом концентрированная серная кислота образует не окрашенный продукт, а желеобразный осадок. Под действием азотной кислоты образуются окрашенные в темно-красный цвет продукты взаимодействия с прометазина и хлорпромазина гидрохлоридами. Окраска переходит в желтую, раствор хлорпромазина гидрохлорида при этом мутнеет. Растворы морацизина гидрохлорида и этацизина в разведенной хлороводородной кислоте после кипячения окрашиваются в сиреневый цвет, но раствор у этацизина мутнеет, а у морацизина гидрохлорида от добавления нитрита натрия окраска переходит в зеленый, а затем в желтый цвет (реакция на морфолиновый цикл).
В качестве реактивов для идентификации используют также красители. Общим реактивом на производные фенотиазина является метиленовый синий, который в виде 0,1%-ного раствора в присутствии концентрированной серной кислоты образует окрашенные продукты реакции. Хлорпромазина гидрохлорид приобретает пурпуровое окрашивание, промазина гидрохлорид — светло-коричневое, прометазина гидрохлорид — пурпурно-коричневое, трифлуоперазина гидрохлорид — серовато-зеленое.
Ацетоновый раствор малеинового ангидрида является групповым реактивом на производные фенотиазина. Продукты реакции приобретают желто-оранжевое окрашивание, максимумы светопоглощения растворов находятся в области 336–360 нм.
Окрашенные в красный цвет комплексные соединения с производными фенотиазина образуют ионы железа (III), ртути (II), кобальта, палладия, платины. Раствор прометазина гидрохлорида после добавления нитрата серебра в 0,002 М растворе серной кислоты после нагревания на водяной бане приобретает вишнево-красное окрашивание. Осадки белого цвета образуют с растворами некоторых производных фенотиазина тиоцианат калия, оксалат аммония, гексацианоферрат (III) калия, а нитропруссид натрия дает красный осадок (прометазина и хлорпромазина гидрохлориды). Производные фенотиазина образуют окрашенные осадки при взаимодействии с тиоцианатоацидокомплексами железа, кобальта и никеля и белые осадки — с тиоцианатоацидокомплексами цинка и кадмия. Осадки растворяются в бензоле, хлороформе, дихлорэтане.
Кобальтинитрит (гексанитрокобальтат) натрия в присутствии уксусного ангидрида образует с производными фенотиазина при нагревании вещества, имеющие красное окрашивание. Трифлуоперазина гидрохлорид в этих условиях окрашивается в зеленый цвет. Раствор иодмонохлорида с прометазина, хлорпромазина гидрохлоридами и трифлуоперазина гидрохлоридом образует бурого цвета осадки. При последующем добавлении насыщенного водного раствора сульфаниловой кислоты и этанола прометазина гидрохлорид приобретает зеленое, а хлорпромазина гидрохлорид и трифлуоперазина гидрохлорид — фиолетовое окрашивание (А.И. Сичко).
Наличие атома серы в молекулах производных фенотиазина устанавливают после прокаливания с карбонатом натрия и нитратом калия. Образовавшийся сульфат-ион обнаруживают в фильтрате, используя в качестве реактива раствор хлорида бария. Атом азота подтверждают с помощью общеалкалоидных реактивов, в частности, раствора иода в иодиде калия (реактив Вагнера-Бушарда).
Трифлуоперазина гидрохлорид с раствором пикриновой кислоты выделяет пикрат, имеющий стабильную температуру разложения (240–243°C). Пикраты могут образовывать и другие производные фенотиазина, в т.ч. прометазина гидрохлорид (160 °C), хлорпромазина гидрохлорид (177 °C) и др. Карбэтоксигруппу в молекулах морацизина гидрохлорида и этацизина обнаруживают по образованию иодоформа после действия раствором иода в щелочной среде:
C2H5OH + 4I2 + 6KOH ¾® CHI3¯ + 5KI + HCOOK + 5H2O
Общим испытанием на производные фенотиазина является реакция осаждения оснований из их водных растворов при действии раствором гидроксида натрия (основание выпадает в виде белого осадка). Осадок отфильтровывают и в фильтрате обнаруживают хлориды по реакции с раствором нитрата серебра.
Атом фтора в молекулах фторсодержащих производных фенотиазина (трифлуоперазина гидрохлорид) обнаруживают после сжигания в кислороде до образования фторид-иона. Его затем открывают цветной реакцией с ализариновым красным C в присутствии нитрата циркония. Смесь этих реактивов (ализаринат циркония) имеет красно-фиолетовое окрашивание. При добавлении фторид-иона оно переходит в желтое (окраска свободного ализарина) (химизм см. ч. 2, гл. 10).
Дифференцировать производные фенотиазина можно с помощью метода ТСХ на пластинках Силуфол УФ-254 в системе растворителей этилацетат–этанол–диэтиламин (17:2:0,5). После хроматографирования и проявления парами иода в зависимости от характера заместителя в положении 2 зоны адсорбции приобретают сине-зеленое (промазина, прометазина, хлорпромазина гидрохлориды) или розово-оранжевое окрашивание (трифлуоперазина гидрохлорид, фторфеназин). Кроме того идентифицировать можно по различающимся средним значениям Rf. Метод ТСХ использован в НД для установления подлинности левомепромазина в таблетках. Основные пятна хроматограмм испытуемого и стандартного растворов должны быть идентичными по размерам, окраске и величине Rf (около 0,7). Этим же методом обнаруживают посторонние примеси при испытании на чистоту производных фенотиазина. Для установления примесей используют, как правило, пластинки Силуфол УФ-254. Хроматографируют восходящим методом параллельно с растворами свидетелей в системе растворителей: гексан-ацетон-диэтиламин (50:30:2) или хлороформ-диэтиламин (9:1). Детектируют хроматограммы в УФ-свете при 254 нм. Допустимое содержание примесей устанавливают по количеству, расположению, размеру и интенсивности пятен на хроматограмме, в сравнении со свидетелями. Суммарное содержание примесей (ФС) не должно превышать у прометазина гидрохлорида 1,5%, хлорпромазина гидрохлорида 2%, морацизина гидрохлорида 1%.
Количественное определение производных фенотиазина выполняют различными вариантами метода титрования в неводных средах. Титрантом во всех случаях является раствор хлорной кислоты. Используя в качестве растворителя ацетон и индикатора раствора метилового оранжевого (в ацетоне), титруют промазина, прометазина, хлорпромазина гидрохлориды. В других случаях растворителем служит ледяная уксусная кислота (трифлуоперазина гидрохлорид), а индикатором — кристаллический фиолетовый. Указанные условия титрования возможны в присутствии ацетата ртути (II).
Для гидрохлоридов 10-алкилпроизводных фенотиазина процесс неводного титрования происходит по следующей схеме:

Используют также (ФС) варианты титрования в неводной среде без добавления ацетата ртути (II). Например, гидрохлориды 10-ацилпроизводных фенотиазина (морацизина гидрохлорид, этацизин) можно оттитровать в смеси муравьиной кислоты, уксусного ангидрида и бензола (1:30:20) с индикатором кристаллическим фиолетовым. Химизм этого процесса рассмотрен на примере определения эфедрина гидрохлорида (см). Не требуется добавления ацетата ртути (II) при определении хлорпромазина гидрохлорида в среде уксусного ангидрида при условии использования в качестве индикатора малахитового зеленого, при титровании прометазина гидрохлорида с индикатором кристаллическим фиолетовым, но в смеси муравьиной кислоты и уксусного ангидрида (1:20), а также промазина гидрохлорида с тем же индикатором в смеси ледяной уксусной кислоты, уксусного ангидрида и бензола (1,5:20:5).
Определить содержание производных фенотиазина можно алкалиметрическим методом, титруя 0,1 М водным раствором гидроксида натрия (индикатор фенолфталеин). Для извлечения выделяющегося органического основания добавляют хлороформ:

Восстановительные свойства производных фенотиазина положены в основу цериметрического определения. Сущность методик заключается в растворении навески (0,02–0,03 г) в 10 мл метанола, нагревании до кипения, охлаждении, прибавлении 10 мл разведенной серной кислоты и титровании 0,1 М раствором сульфата церия (IV) до исчезновения появляющегося после добавления первых капель титранта окрашивания. Таким образом, титрование выполняют без использования индикатора.
Иодометрическое определение хлорпромазина гидрохлорида основано на образовании полииодида. Описано его броматометрическое определение, суть которого состоит в титровании 0,1 М раствором бромата калия раствора навески в 2 М растворе хлороводородной кислоты в присутствии бромида калия до обесцвечивания появляющейся красной окраски. Иодхлорометрическое определение промазина и хлорпромазина гидрохлоридов заключается в выделении эквивалентного количества иода после отделения и разложения образовавшегося продукта присоединения (RN)2×IСl:
(RN)2 · ICl + KI ——→ 2RN + KCl + I2
Количественное определение левомепромазина выполняют методом двухфазного титрования с использованием титранта 0,01 М раствора лаурилсульфата натрия и индикатора диметилового желтого в присутствии хлороформа.
Известны также способы косвенного комплексонометрического титрования производных фенотиазина. Количественное определение производных фенотиазина в лекарственных формах выполняют спектрофотометрическим методом (промазина, хлорпромазина гидрохлориды, левомепромазин и др.) в указанных выше максимумах поглощения. Широко используют для фотоколориметрического определения цветные реакции, основанные на окислении и комплексообразовании. Точность, сопоставимую с титриметрическими методами, позволяет достигнуть дифференциальное спектрофотометрическое и экстракционно-фотометрическое определение с тиоцианатоацидокомплексом кобальта (А.И.Сичко, В.Е.Годяцкий).
Хранение и применение
Все производные фенотиазина, хранят по списку Б с учетом их гигроскопичности и способности легко окисляться, в банках темного стекла, плотно закрытых пробками, залитых парафином, в сухом, защищенном от света месте.
При длительном пребывании на воздухе прометазина гидрохлорид медленно окисляется и приобретает синее окрашивание. Он постепенно разлагается во влажной атмосфере даже в темноте, особенно при повышенной температуре. На примере прометазина гидрохлорида показано, что при хранении его раствора в ампулах происходит разложение с образованием осадка и летучих веществ, имеющих характерный запах. Осадок представляет собой хлорид фенотиазина. Запах обусловлен изменениями в алифатической части молекулы, которая разлагается до формальдегида, ацетальдегида и диметиламина. Установлено, что 10-ацилфенотиазины под влиянием внешних факторов (свет, кислород, влага) разлагаются с образованием фенотиазина и продуктов его окисления. Хлорпромазина гидрохлорид темнеет при длительном воздействии света. Он разрушается даже в темноте при влажной атмосфере.
Производные фенотиазина, обладают способностью проникать в организм через дыхательные пути, кожу и слизистую оболочку. При этом они вызывают аллергические реакции (зуд и отечность слизистых оболочек, кожи рук, снижение артериального давления, состояние депрессии и т.д.). Поэтому следует строго соблюдать технику безопасности в работе, исключая возможность попадания лекарственных веществ на кожу и слизистые оболочки. Работать необходимо под тягой в резиновых перчатках. По окончании работы руки нужно вымыть холодной водой (без мыла), слегка подкисленной, чтобы не допустить выделения на коже оснований фенотиазиновых производных.
Нейролептические и седативные средства, производные фенотиазина — промазина гидрохлорид, хлорпромазина гидрохлорид, трифлуоперазина гидрохлорид назначают при психических заболеваниях. Промазина гидрохлорид и хлорпромазина гидрохлорид применяют внутрь в дозах 0,025–0,05 г (парентерально в виде 2,5%-ных растворов). Трифлуоперазина гидрохлорид более активен, поэтому его применяют внутрь по 0,005 г). У прометазина гидрохлорида более выражена противогистаминная активность. Поэтому его используют при аллергических заболеваниях внутрь по 0,025 г, а внутримышечно или внутривенно в виде 2,5%-ного раствора. Левомепромазин — нейролептическое и противорвотное средство, обладающее также седативной и противогистаминной активностью. Назначают его при психозах, неврозах, невритах различной этиологии внутрь в таблетках по 0,025 г и внутримышечно 2,5%-ные растворы по 1 мл. Морацизина гидрохлорид и этацизин применяют при нарушениях сердечного ритма внутрь в таблетках по 0,05–0,1 г или внутривенно в виде 2,5%-ного раствора по 2 мл.
Производным фенотиазина является также сложный эфир флуфеназина деканоат (Fluphenazine Decanoate), представляющий собой 2-трифторметил-10-{3-[1-(b-каприноил-оксиэтил)-пиперазинил-4]-пропил}-фенотиазин:

Флуфеназина деканоат отличается от других нейролептиков этого ряда тем, что обладает пролонгированным эффектом за счет этерификации спиртовой группы каприновой кислотой. Этерификация увеличивает относительную молекулярную массу и придает высокую липофильность. В виде 2,5%-ного раствора в масле в зависимости от дозы он действует до 1–2 недель и более.
ГЛАВА 71.
|
Просмотров 8120 |
|
|
