
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Особенности окисления ненасыщенных жирных кислот
|
|
Ненасыщенные жирные кислоты в значительных количествах входят в состав животных и растительных клеток, что определяется их биологи-ческой ролью. В отличие от D-стереоизомеров еноильных промежуточных продуктов процесса β-окисления природные ненасыщенные жирные кислоты представлены L-стереоизомерами. В полиненасыщенных жирных кислотах, помимо этого, двойные связи не занимают того положения, в котором они могли бы подвергаться действию еноил-КоА-гидратазы. Поэтому их окисление требует дополнительных ферментативных стадий.
Существуют два дополнительных фермента, присутствие которых позволяет использовать ненасыщенные жирные кислоты в процессе β-окис-ления. Как можно видеть на примере олеиновой кислоты, первоначально она вступает в три последовательные стадии цикла β-окисления, вследствие чего укорачивается на шесть углеродных атомов, которые используются для образования трех ацетильных радикалов в молекулах ацетил-КоА. Другим продуктом распада олеиновой кислоты при этом становится 12-углеродная ненасыщенная жирная кислота с двойной связью между третьим и четвертым углеродными атомами в cis-конфигурации (рис. 104). Этот продукт не может подвергаться дальнейшим превращениям в еноил-КоА-гидратазной реакции процесса β-окисления (рис. 101).
Данный промежуточный продукт окисления ненасыщенной жирной кислоты под действием еноил-КоА-изомеразы превращается в trans-изо-мер, в котором двойная связь перемещается от третьего к второму углеродному атому. Продукт реакции приобретает способность вступать в реакцию гидратации, катализируемую еноил-КоА-гидратазой.
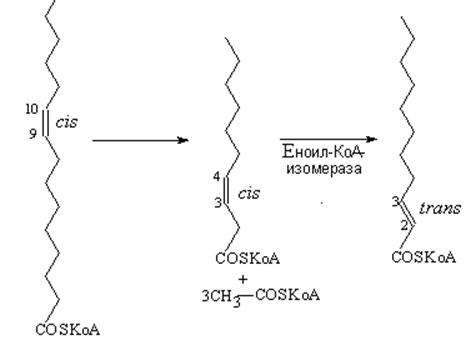
Рисунок 104 –Особенности окисления ненасыщенной жирной кислоты
(пальмитоолеиновой кислоты) в процессе β-окисления
Сначала происходит распад пальмитоолеиновой кислоты с образованием трех молекул ацетил – КоА и 3,4-cis-еноил-КоА (С10). Образовавшийся cis-изомер еноил-КоА под действием еноил-КоА-изомеразы превращается в trans-изомер. trans-Еноил-КоА вступает в цикл β-окисления на уровне еноил-КоА-гидратазной реакции.
Окисление полиненасыщенных жирных кислот требует участия дополнительного фермента – эпимеразы.
Синтез высших жирных кислот
Биосинтез высших жирных кислот происходит в цитозоле животной клетки, так как именно в этом внутриклеточном компартменте локализуется комплекс ферментов, катализирующий отдельные стадии данного процесса. В растительных клетках биосинтез жирных кислот происходит в хлоропластах.
Предшественником образования высших жирных кислот является ацетил-КоА. Мощными поставщиками данного метаболита служат следующие процессы:
1. Окислительного декарбоксилирования пирувата.
2. Окислительного распада аминокислот.
3. β-Окисления высших жирных кислот.
Все эти процессы происходят внутри митохондрий. Однако внутренняя митохондриальная мембрана непроницаема для ацетил-КоА. В связи с этим его транспорт из митохондрий в цитоплазму осуществляется с помощью особого механизма переноса. Суть переноса ацетил-КоА в цитоплазму заключается в следующем.
В митохондриальном матриксе ацетил-КоА в цитратсинтазной реакции цикла трикарбоновых кислот взаимодействует с оксалоацетатом. При этом в качестве продукта реакции образуется лимонная кислота:

Лимонная кислота при помощи особого белкового переносчика трикарбоновых кислот транспортируется через внутреннюю митохондриальную мембрану в межмембранное пространство митохондрий и далее – в цитоплазму. В цитоплазме клетки она распадается под действием фермента АТФ – цитратлиазы:

Таким образом, в двух сопряженных реакциях, которые протекают в различных компартментах клетки и при участии переносчика трикарбоксилатов, ацетил-КоА транспортируется из митохондрий в цитоплазму. Этот процесс является энергозависимым, так как связан с использованием АТФ в цитратлиазной реакции.
Цитозольный ацетил-КоА подвергается карбоксилированию в реакции, катализируемой ацетил-КоА-карбоксилазой:
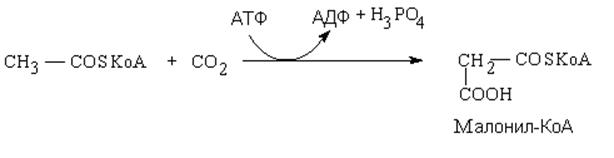
Фермент ацетил-КоА-карбоксилаза представляет собой сложный белок, у которого в качестве простетической группы используется остаток фосфорилированного биотина (витамина Н). Реакция, катализируемая этим энзимом, практически необратима, что связано сопряженным с ней гидролизом АТФ. Продуктом этой реакции является малонил-КоА, ключевой продукт синтеза высших жирных кислот.
Ацетил-КоА-карбоксилазная реакция – это лимитирующая стадия процесса биосинтеза высших жирных кислот. Ацетил-КоА-карбоксилаза представляет собой аллостерический фермент. В качестве его активатора выступает лимонная кислота, а ингибитора – конечный продукт биосинтеза высших жирных кислот – пальмитоил-КоА.
Все ферменты, катализирующие последующие стадии синтеза жирных кислот, связаны в единый полиферментный комплекс, получивший название синтаза высших жирных кислот. В его состав входят семь различных энзимов в определенных количественных соотношениях друг с другом. В клетках позвоночных животных свойства всех отдельных ферментов комплекса выполняет единственный полипептид, на котором имеется семь различных активных центров. При этом в состав синтазы высших жирных кислот в них входит две субъединицы, представленные такими полипептидами.
Центральное место в комплексе занимает ацилпереносящий белок (АПБ). АПБ последовательно соединяется с промежуточными продуктами биосинтеза и переносит их с активного центра одного фермента на другой (рис. 105).

Рисунок 105 – Схема строения синтазы высших жирных кислот
АПБ представляет собой сложный белок, имеющий сравнительно небольшую молекулярную массу. Его небелковая часть (простетическая группа) представляет собой 4-фосфопантотеин – фосфорилированное производное витамина ВЗ (пантотеновой кислоты), с которым связан остаток тиоэтаноламина:

Простетическая группа АПБ связывается с его полипептидной цепью через остаток серина.
SH-группа простетической группы АПБ участвует в связывании малонильного остатка. Важное значение в синтезе высших жирных кислот приобретает еще одна сульфгидрильная группа, входящая в состав цистеинового радикала одного из ферментов синтазного комплекса. Учитывая значения различных SH-групп в синтезе высших жирных кислот, активный синтазный комплекс можно представить как (рис. 106)

Рисунок 106 – Схематическое изображение полиферментного
комплекса синтеза высших жирных кислот (СВЖК)
Началу синтеза высшей жирной кислоты предшествует присоединение исходных субстратов (ацетил-КоА и малонил-КоА) к синтазному комплексу (рис. 107):
Процесс присоединения субстратов происходит с участием ферментов синтазного комплекса – АПБ-ацетилтрансферазы и АПБ-малонил-trans-феразы. В связанном с ацетильным и малонильным радикалами состоянии комплекс готов к началу процесса синтеза высшей жирной кислоты.

Рисунок 107 – Присоединение субстратов к синтазе высших жирных кислот
На начальной стадии биосинтеза высших жирных кислот происходит конденсация ацетильной и малонильной групп, с образованием ацетоацетильного промежуточного продукта. Реакция катализируется ферментом
3-кетоацил-АПБ-синтазой. В ходе этой реакции происходит выделение молекулы СО2, которая в свое время была использована для синтеза малоновой кислоты (рис. 108).
Образованный 3-кетоацил связан с SH-группой небелкового компонента АПБ. Вторая активная SH-группа (цистеиновая) синтазного комплекса при этом оказывается в восстановленном состоянии.
В следующей реакции происходит восстановление карбонильной группы 3-кетоацил-АПБ. Реакция катализируется 3-кетоацил-АПБ-редуктазой. Этот фермент представляет собой пиридинзависимую дегидрогеназу, у которой в качестве кофермента используется восстановленный НАДФ. В качестве продукта восстановления при этом образуется 3-гидро-ксиацил-АПБ. В следующей реакции он подвергается дегидратации при помощи фермента 3-гид-роксиацил-АПБ-дегидратазы с образованием непредельного производного жирной кислоты – гноил-АПБ. В заключительной реакции цикла синтеза гноил-АПБ восстанавливается под действием пиридинзависимого энзима – еноил-АПБ-редуктазы. В качестве кофермента этот фермент использует восстановленный НАДФ. Продукт редуктазной реакции представляет собой остаток короткоцепочной жирной (масляной) кислоты – бутирил-КоА.

Рисунок 108 – Цикл синтеза высших жирных кислот на синтазном
полиферментном комплексе
Образованный бутирильный радикал переносится с АПБ на цистеиновую SH-группу синтазного комплекса. К освободившейся при этом сульфгидрильной группе АПБ присоединяется новый малонильный остаток (рис. 109).

Рисунок 109 – Перенос бутирильного остатка на цистеиновую
сульфгидрильную группу синтетазного комплекса
После того как в синтазном комплексе функциональные сульфгидрильные группы оказываются связанными с бутирильным и малонильным радикалами, начинается новый цикл синтеза высшей жирной кислоты. В процессе него происходит образование остатка 6-углеродной кислоты. Цикл синтеза высшей жирной кислоты неоднократно повторяется. В результате происходит последовательное нарастание длины ацильного (жирнокислотного) радикала на два углеродных атома. После образования продукта, содержащего в своем составе 16–18 углеродных атомов (пальмитиновой или стеариновой кислот), синтез жирной кислоты прекращается. Синтезированная молекула жирной кислоты отщепляется от АПБ под действием фермента гидролазы (рис. 110):

Рисунок 110 – Освобождение пальмитиновой кислоты
от синтазного комплекса
Суммарное уравнение процесса синтеза высших жирных кислот на примере пальмитиновой кислоты имеет вид

Учитывая, что предшественником малонил-КоА является ацетил-КоА, балансовое уравнение можно представить как

Из балансового уравнения реакции видно, что процесс биосинтеза ВЖК является энергозависимым. Для его энергетического обеспечения используются АТФ и восстановленный НАДФ.
Продуктами синтеза высших жирных кислот на синтазном комплексе являются жирные кислоты с четным числом углеродных атомов - пальмитиновая и стеариновая кислоты. Далее они могут использоваться в процессах образования жирных кислот с большим числом углеродных атомов (до 22–26), а также ненасыщенных жирных кислот.
Обмен стеринов
Из всех известных стеринов особенно широкое распространение имеет представитель животного происхождения – холестерин. Холестерин выполняет разнообразные функции. Он выступает в роли компонента липидного бислоя биологических мембран, предшественника витамина D, стероидных гормонов и желчных кислот в организме животных.
Большая часть свободного холестерина входит в состав клеточных мембран и миелиновых оболочек нервных проводников.
Биосинтез холестерина условно подразделяется на четыре стадии:
I. Биосинтез мевалоновой кислоты.
II. Образование сквалена из мевалоновой кислоты.
III. Циклизация сквалена с образованием ланостерина.
IV. Превращение ланостерина в холестерин.
Исходным субстратом для биосинтеза холестерина является ацетил-КоА. В результате цепи последовательных ферментативных превращений он через стадию образования 3-гидрокси-3-метилглутарил-КоА трансформируется в мевалоновую кислоту (рис. 111).

Рисунок 111 – Образование мевалоновой кислоты аз ацетил-КоА
На следующей стадии синтеза холестерина происходит фосфорилирование мевалоновой кислоты за счет АТФ и последующее образование ряда фосфорилированных промежуточных продуктов (рис. 112). При декарбоксилировании одного из них образуется изопентилпирофосфат – активная изопреновая единица. Изопентилпирофосфат принимает участие не только в процессе синтеза холестерина. Он выступает также в качестве промежуточного продукта синтеза каротиноидов, боковых цепей убихинона (коэнзима Q), витаминов К и Е.

Рисунок 112 – Основные этапы образования сквалена из
мевалоновой кислоты
В процессе синтеза холестерина часть изопентилпирофосфата изомеризуется в диметилаллилпирофосфат. Конденсация этих двух соединений (изопентинилпирофосфата и диметилаллилпирофосфата) приводит к образованию 10-углеродного промежуточного продукта синтеза холестерина – геранилпирофосфата. Геранилпирофосфат соединяется с новой молекулой изопентенилпирофосфата с образованием фарнезилпирофосфата, содержащего 15 атомов углерода. Две молекулы фарнезилпирофосфата, соединяясь “голова к голове”, теряют пирофосфатный остаток и образуют сквален.
Молекула сквалена состоит из 30 атомов углерода. На стадии образования сквалена завершается анаэробная фаза биосинтеза холестерина. Третья стадия процесса является аэробной и требует присутствия кислорода. На ней происходит окислительная циклизация сквалена, сопровождающаяся образованием первого циклического промежуточного продукта – ланостерина. Ланостерин имеет гидроксильную группу в положении 3 циклопентанпергидрофенантренового остатка, а также три “лишние”, в сравнении с холестерином, метильные группы. Впоследствии эти метильные группы окисляются до карбоксильных, которые удаляются путем декарбоксилирования. В результате всех этих превращений образуется ряд промежуточных продуктов стероидной природы (зимостерин, десмостерин), которые выступают в роли непосредственных предшественников образования холестерина. При восстановлении десмостерина образуется свободный холестерин:

Ланостерин
В растениях сквален циклизируется с образованием стигмастерола, а в грибах – эргостерола, которые в свою очередь выступают в качестве предшественников синтеза растительных стеринов (фитостеринов) и стеринов грибов.
Балансовое уравнение процесса биосинтеза холестерина можно представить как

Из него видно, что из 18 молекул ацетил-КоА образуется одна молекула холестерина. В качестве донора водорода в редуктазных реакциях используется восстановленный НАДФ, а источника кислорода – молекулярный кислород.
Все промежуточные продукты биосинтеза холестерина нерастворимы в воде, поэтому в процессе синтеза они находятся в связанном со стеринпереносящими белками состоянии.
Синтез холестерина регулируется по принципу отрицательной обратной связи. Основным регуляторным звеном этого процесса является 3-гидрокси-3-метилглутарил-КоА-редуктазная реакция.
Распад холестерина не сопровождается разрушением циклопентанпергидрофенантренового фрагмента молекулы и образованием углекислого газа и воды в качестве конечных продуктов. Основные пути утилизации холестерина в организме человека и животных связаны с его превращением в желчные кислоты, витамин D3 и стероидные гормоны.
Важную роль в обмене липидов играет процесс их перекисного окисления (ПОЛ).
|
Просмотров 4094 |
|
|
