
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Пути обезвреживания аммиака в живых организмах
|
|
К основным путям обезвреживания (детоксикации) аммиака относятся процессы, связанные с его использованием для:
· образования амидов аминокислот (аспарагина и глутамина);
· восстановительного аминирования α-кетоглутаровой кислоты;
· биосинтеза мочевины.
В процессе образования амидов аминокислот происходит связывание аммиака с глутаминовой и аспарагиновой кислотами. Ниже представлена реакция образования глутамина, катализируемая глутаминсинтетазой. В качестве продукта этой реакции образуется стандартная аминокислота – глутамин. Аналогичным образом аммиак используется для синтеза аспарагина.

Некоторая часть аммиака используется для восстановительного аминирования α-кетоглутаровой кислоты. Реакция восстановительного аминирования представляет собой обращение окислительного дезаминирования глутаминовой кислоты, катализируемого глутаматдегидрогеназой. Однако в направлении связывания аммиака у глутаматдегидрогеназы в качестве кофермента используется восстановленный НАДФ.

Основным путем обезвреживания аммиака в организме человека и животных является процесс мочевинообразования. Образующаяся в нем мочевина представляет собой нетоксичный конечный продукт азотистого обмена.
Наиболее интенсивно синтез мочевины происходит в печени животных. С незначительной скоростью он идет также в почках и мозге. Однако вклад этих органов в общий баланс мочевинообразования невысок.
Еще в прошлом веке Н. В. Ненцкий и С. С. Салазкин показали, что в печени происходит образование мочевины из аммиака и углекислоты. Однако только в 1952 г. Г. Кребс и К. Хензелайт детально изучили этот процесс и ввели представление о цикле мочевинообразования.
Начальной реакцией процесса мочевинообразования является синтез богатого энергией соединения (макроэргического фосфата) – карбамоилфосфата (рис. 121). Далее карбамоилфосфат соединяется с нестандартной аминокислотой – орнитином, в результате чего образуется новая нестандартная аминокислота – цитруллин. В следующей реакции цитруллин взаимодействует с аспарагиновой кислотой, образуя аргининосукцинат. Аргининосукцинат распадается на аргинин и фумаровую кислоту. Образовавшийся аргинин под воздействием фермента аргиназы распадается до мочевины и орнитина.
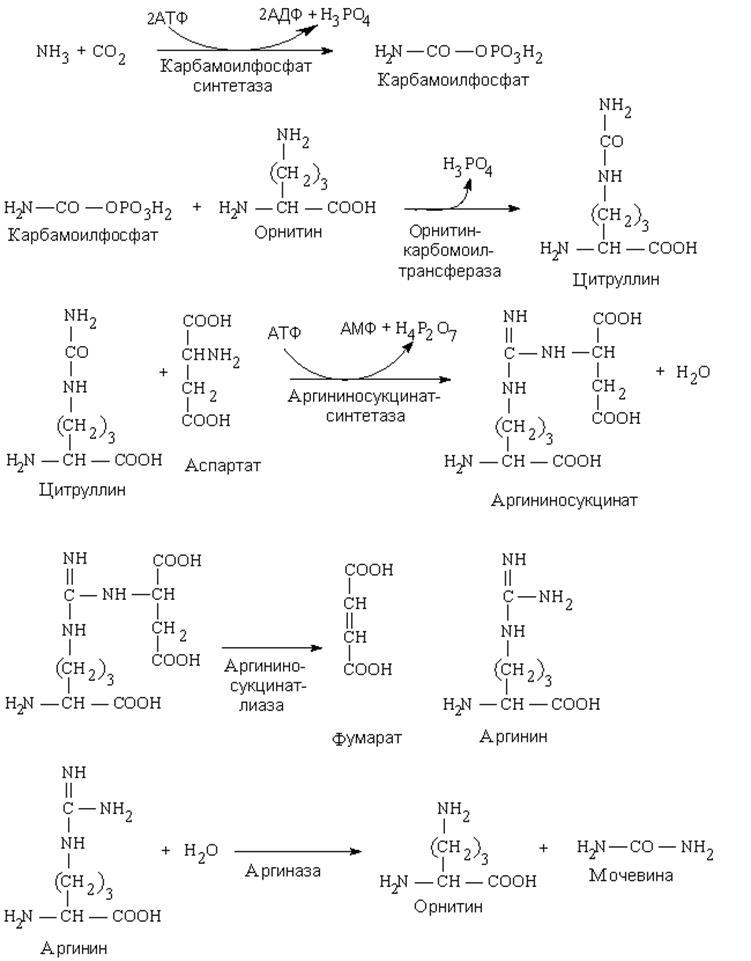
Рисунок 121 – Цикл мочевинообразования
Синтезированная мочевина выделяется из организма через почки, а орнитин вновь вовлекается в реакцию взаимодействия с карбамоилфосфатом. Образовавшаяся в орнитиновом цикле фумаровая кислота, затем может подвергаться окислительным превращениям в цикле трикарбоновых кислот. Она используется для образования яблочной кислоты, которая далее в малатдегидрогеназной реакции окисляется в оксалоацетат. В свою очередь оксалоацетат может вовлекаться в реакцию переаминирования с глутаминовой кислотой, продуктом которой является аспарагиновая кис-лота – один из субстратов орнитинового цикла. Таким образом, фумаровая кислота выступает в качестве своеобразного связующего звена между циклом мочевины с циклом трикарбоновых кислот (рис. 122).

Рисунок 122 – Взаимосвязь между циклом мочевины
и циклом трикарбоновых кислот
Ниже приведено балансовое уравнение цикла мочевины:
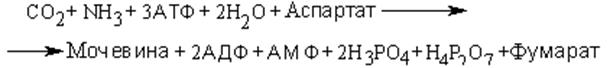
Из него виден энергозависимый характер данного процесса. При образовании одной молекулы мочевины происходит использование трех молекул АТФ.
В последнее время доказано, что мочевина является не просто конечным продуктом азотистого обмена, смысл образования которого сводится только к детоксикации аммиака. Установлено, что она обладает выраженной биологической активностью, выступая в роли одного из важнейших водорастворимых антиоксидантов.
|
Просмотров 2303 |
|
|
