
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Обмен фенилаланина и тирозина
|
|
Феналаланин является незаменимой аминокислотой. Единственный его источник для человека – пищевые белки. Основные пути утилизации фенилаланина представлены на рис. 124.
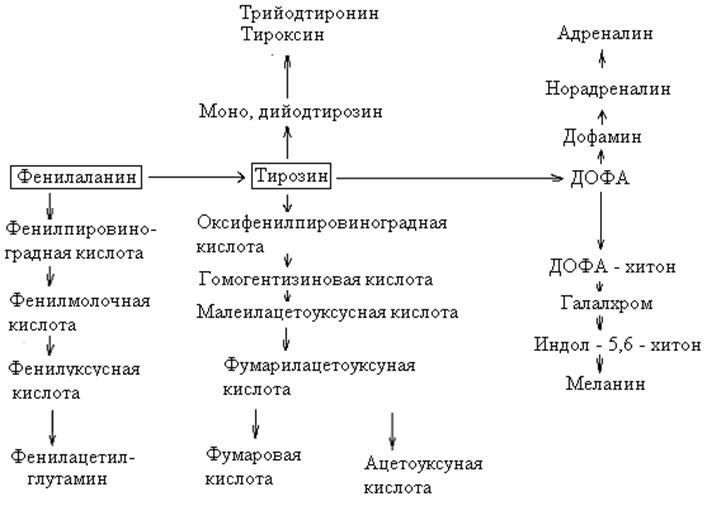
Рисунок 124 – Схема путей метаболизма фенилаланина и тирозина
Как видно из представленного рисунка, основной путь обмена фенилаланина заключается в его окислении в тирозин. Тирозин представляет собой заменимую аминокислоту. Пути его метаболизма значительно шире, чем у фенилаланина. Он используется для синтеза белков, образования катехоламинов, гормонов щитовидной железы (тироксина, трийодтиронина), пигмента меланина и подвергается распаду до углекислого газа и воды.
Начальным этапом метаболизма тирозина является его трансаминирование с образованием оксифенилпировиноградной кислоты. Последний под действием специфической медьсодержащей окcидазы подвергается окислению, гидроксилированию, декарбоксилированию и внутримолекулярному переносу боковой цепи с образованием гомогентизиновой кислоты. Окисление гомогентизиновой в малеилацетоуксусную кислоту катализируется оксидазой гомогентизиновой кислоты. Малеилацетоуксусная кислота изомеризуется в фумарилацетоуксусную, которая далее гидролизуется до фумаровой и ацетоуксусной кислот. Образовавшиеся продукты могут окисляться до конечных продуктов обмена (CO2 и H2O) или использоваться в качестве предшественников глюкозы и жирных кислот.
Другой путь метаболизма тирозина связан с образованием биологически активных веществ – катехоламинов. Под действием фермента тирозиназы происходит гидроксилирование тирозина с образованием диоксифенилаланина (ДОФА). ДОФА декарбоксилируется, в результате чего синтезируется дофамин – предшественник норадреналина и адреналина.
Тирозин используется также для синтеза пигмента меланина. Меланин представляет собой группу полимеров, которая обеспечивает пигментацию кожи, глаз, волос.
Еще одним путем метаболизма тирозина является его использование в биосинтезе гормонов щитовидной железы (Т3 и Т4).
Обмен триптофана
Подобно фенилаланину триптофан является незаменимой аминокислотой. Его распад может происходить в трех различных путях: кинурениновом, серотониновом и в пути, связанном с образованием индолилуксусной кислоты (рис. 125).
При гидроксилировании триптофана образуется 5-окситриптофан, который используется для синтеза биологически активного вещества – серотонина.
Кинурениновый путь распада триптофана начинается с его окисления до формилкинуренина под воздействием триптофан-2,3-диоксигеназы. Формилкинуренин в цепи последовательных ферментативных превращений распадается с образованием продуктов, которые могут использоваться для синтеза НАД.

Рисунок 125 – Схема основных путей использования триптофана
В третьем пути катаболизма триптофан превращается в индолилуксусную кислоту. Данный продукт превращения триптофана обладает выраженной ростстимулирующей активностью у растений.
Обмен глицина
Глицин относится к заменимым аминокислотам. Он может синтезироваться либо из треонина под действием треонинальдолазы, либо из серина под действием сериноксиметилтрансферазы, коферментом которой является тетрагидрофолиевая кислота (ТГФК).
Глицин принимает участие в самых различных путях метаболизма
(рис. 126). Из представленного рисунка видно, что он используется в белковом, липидном, углеводном обменах, синтезе мононуклеотидов, образовании глютатиона и др.

Рисунок 126 – Схема основных путей использования глицина
 Основным путем катаболизма глицина является его окислительное расщепление до CO2, NH3 и метиленовой группы (-CH2-), которая присоединяется к тетрагидрофолату. Реакция легко обратима и катализируется глицинсинтазой:
Основным путем катаболизма глицина является его окислительное расщепление до CO2, NH3 и метиленовой группы (-CH2-), которая присоединяется к тетрагидрофолату. Реакция легко обратима и катализируется глицинсинтазой:
 Биологическое значение этого пути состоит в образовании активного одноуглеродного (метиленового) фрагмента , используемого в синтезе тимидиловой кислоты, пуриновых нуклеотидов, метионина и др.
Биологическое значение этого пути состоит в образовании активного одноуглеродного (метиленового) фрагмента , используемого в синтезе тимидиловой кислоты, пуриновых нуклеотидов, метионина и др.
Существует специфический фермент – глициноксидаза, катализирующий реакцию окислительного дезаминирования глицина. Одним из продуктов реакции, катализируемой этим ферментом, является глиоксиловая кислота:
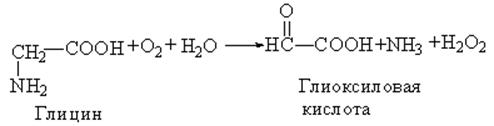
Глиоксилиловая кислота может подвергаться декарбоксилированию с образованием муравьиной кислоты и углекислого газа:
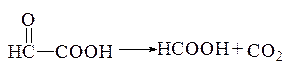 | |||||
 | |||||
 | |||||
Муравьиная кислота подвергается восстановлению в
при участии восстановленного НАДФ и ТГФК или окислению с образованием щавелевой кислоты.
Глицин участвует в образовании s-аминолевулиновой кислоты в процессе биосинтеза гема. Поскольку эта аминокислота принимает участие в синтезе серина, который легко превращается в пировиноградную кислоту, она выступает в качестве одного из связующих звеньев между углеводным и липидным обменами.
Контрольные вопросы
1. Классификация протеолитических ферментов и их представители.
2. Каков механизм образования соляной кислоты в желудке и ее значение?
3. Укажите особенности переваривания белков в кишечнике.
4. Почему при употреблении человеком в пищу только растительных белков происходит уменьшение массы организма?
5. Перечислите и охарактеризуйте общие пути катаболизма аминокислот.
6. Почему дезаминирование многих аминокислот связано с процессом окислительного дезаминирования?
7. Каким образом происходит детоксикация аммиака?
8. Укажите значение орнитинового цикла.
|
Просмотров 3748 |
|
|
