
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Этановая кислота 2-метилпропановая бутен-3-овая кислота
|
|
кислота
Для двухосновных кислот название строится так же, с окончанием -диовая:
НООС–СН2–СН2-СООН (бутандиовая кислота).
В названиях ароматических кислот в качестве родоначальной структуры используется бензойная кислота.
 |



бензойная 2-метил- 3-метил- 4-метил-
кислота бензойная бензойная бензойная
кислота кислота кислота
Карбоновые кислоты известны с давних времен, поэтому для многих из них прочно утвердились тривиальные названия. Происхождение таких названий, как правило, связано с природными объектами, из которых они выделены.
Рассмотрим наиболее широко распространенные одноосновные предельные и непредельные карбоновые кислоты.
| Формула | Тривиальное | ИЮПАК |
| название | ||
| Н-СООН | Муравьиная | метановая |
| СН3-СООН | Уксусная | этановая |
| СН3-СН2-СООН | Пропионовая | пропановая |
| СН3-СН2-СН2-СООН | Масляная | бутановая |
| СН3-СН-СООН ½ СН3 | Изомасляная | 2-метилпропановая |
| СН3-СН2-СН2-СН2-СООН | Валериановая | пентановая |
| СН2=СН-СООН | Акриловая | пропеновая |
Высшие жирные кислоты (ВЖК)
 Предельные:
Предельные:
Пальмитиновая С15Н31СООН

Стеариновая С17Н35СООН
 Непредельные:
Непредельные:
Олеиновая С17Н33СООН
 |
Линолевая С17Н31СООН

Линоленовая С17Н29СООН

Арахидоновая С19Н31СООН
ВЖК имеют наиболее выгодную зигзагообразную конформацию углеродной цепи; ненасыщенные ВЖК содержат одну или несколько двойных связей. Как правило, число атомов углерода в них четное.
Полиненасыщенные ВЖК, в отличие от насыщенных, не синтезируются в организме человека. Они являются незаменимыми и должны поступать с пищей, в основном с растительными маслами. Для профилактики и лечения некоторых заболеваний, связанных с недостатком ненасыщенных ВЖК, применяют препарат «Линетол», представляющий собой смесь этиловых эфиров жирных кислот, получаемых из льняного масла.
Важную роль в организме играет арахидоновая кислота. Она является предшественником эйкозаноидов – сильнодействующих биорегуляторов клетки.
ВЖК входят в состав жиров (триацилглицеролов), выполняющих резервную функцию, а также фосфолипидов, составляющих основу мембраны клетки.
Изомерия
Структурная изомерия карбоновых кислот обусловлена разветвлением углеродного скелета (бутановая и 2-метилпропановая кислота) и взаимным расположением заместителей и карбоксильной группы в ароматических кислотах (три изомера метилбензойной кислоты).
Стереоизомерия карбоновых кислот обусловлена различным расположением заместителей относительно двойной связи для непредельных кислот или относительно плоскости кольца для алициклических с образованием цис- и транс-изомеров. Простейшая непредельная бутендиовая кислота существует в виде стереоизомеров: цис-изомера – малеиновой кислоты и транс-изомера – фумаровой:
 | |||
 | |||
Малеиновая фумаровая кислота
кислота транс–изомер
цис–изомер
Ненасыщенные ВЖК чаще всего имеют цис-конфигурацию:

Линолевая кислота
Большей энергетической устойчивостью обладают транс-изомеры.
Физические свойства.
Молекулы карбоновых кислот полярны. Они способны, как и спирты, образовывать водородные связи. Температура кипения кислот значительно выше, чем спиртов и альдегидов, так как кислоты образуют ассоциаты за счет межмолекулярных водородных связей линейной и циклической структуры.
 |  | ||||
 | |||||

 ……
……

…… ... … … …
димерный ассоциат линейный ассоциат
Низшие карбоновые кислоты (С1 – С9) представляют собой жидкости, высшие алифатические и ароматические кислоты – твердые вещества. Первые гомологи – муравьиная, уксусная и пропионовая кислоты – обладают резким раздражающим запахом, при попадании на слизистые оболочки вызывают ожоги, с водой смешиваются в любых соотношениях. По мере увеличения гидрофобной углеводородной части молекулы растворимость в воде уменьшается. Двухосновные кислоты – бесцветные кристаллические вещества, растворимые в воде.
Химические свойства
Карбоксильная группа карбоновых кислот имеет сложное строение: она состоит из карбонильной группы С=О и гидроксильной группы –ОН, которые влияют друг на друга.
Благодаря +M –эффекту ОН-группы в карбоксильной группе возникает рp -сопряжение, происходит выравнивание электронной плотности в ней и сведение полярности карбонильной группы до минимума. Этим объясняется инертность карбонильной группы в кислотах. +М –эффект гидроксильной группы объясняет также смещение электронной плотности в ней в сторону более электроотрицательного атома кислорода и диссоциацию кислот.
 |
(- I) – эффект гидроксильной группы поляризует связь С®ОН и делает возможным ее отщепление: группа ОН может отщепляться, что обусловливает реакции нуклеофильного замещения. Таким образом, главные реакции идут либо за счет замещения ОН - группы, либо за счет водорода этой группы.
1. Кислотные свойства Сила карбоновых кислот зависит от стабильности аниона, образующегося после отрыва протона. Стабильность аниона определяется, прежде всего, степенью делокализации отрицательного заряда: чем выше степень делокализации, тем стабильнее анион.
В карбоксилат-анионе заряд делокализуется по сопряженной системе, т. е. равномерно распределяется между двумя атомами кислорода карбоксилат–аниона, что придает ему стабильность:


|


 O
O
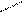

 R – C
R – C  (-)
(-) 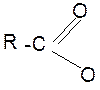


 (–) O
(–) O
В рамках класса сила кислот зависит от строения углеводородных радикалов и заместителей в них. Электронодонорные заместители ослабляют кислотные свойства, так как дестабилизируют карбоксилат–анион; электроноакцепторные заместители, оттягивая электронную плотность, способствуют делокализации заряда в карбоксилат – анионе и тем самым стабилизируют его, т.е. усиливают кислотные свойства.
Так, при введении в углеводородный радикал уксусной кислоты атомов хлора кислотность будет увеличиваться за счет электроноакцепторных свойств атома хлора:
Cl
СН3®СООН < СН2СООН < СlСНСООН < СlССООН
¯ ¯ ¯
Сl Cl Cl
рКа 4,76 2,85 1,25 0,66
Ароматические кислоты имеют более сильные кислотные свойства, чем незамещенные алифатические (для бензойной кислоты С6Н5-СООН рКа=4,19) – сказывается электронное влияние фенильного радикала (-I).
Кислотные свойства проявляются в реакции нейтрализации:
СН3 – СООН + NaOH  CH3COONa + H2O
CH3COONa + H2O
2. Реакции нуклеофильного замещения (SN ):
 а) реакция этерификации:
а) реакция этерификации:
|
 Механизм реакции:
Механизм реакции:

 ..
..
НОС2Н5 -Н2О
 + Н+
+ Н+ 


 | |||
 | |||
-Н+


Реакция этерификации – обратимый процесс: прямая реакция – образование сложного эфира, обратная – его кислотный или щелочной гидролиз. Чтобы сдвинуть равновесие вправо, необходимо из реакционной смеси удалить воду
б) образование галогенангидридов:
Среди галогенангидридов наибольшее значение имеют хлорангидриды, которые получают при действии хлоридов фосфора (III) или фосфора (V):
 | |||
 |
 + PCl5 + POCl3 + HCl
+ PCl5 + POCl3 + HCl
хлористый ацетил
в) образование ангидридов кислот:
При действии сильных водоотнимающих агентов (P2O5, Al2O3) образуются ангидриды кислот:


___
½½ Al2O3 + H2O

 ½½
½½
Большое практическое значение имеет уксусный ангидрид, используемый для получения волокон (ацетатный шелк), многих лекарственных веществ. Применяется также для ацетилирования соединений.
Галогенангидриды и ангидриды очень реакционноспособны. При взаимодействии галогенангидридов с соединениями, содержащими атом металла или активный атом водорода, происходит замена его кислотным остатком. Подобные реакции называются ацилированием, в частности ацетилированием, если в молекулу входит ацетил, остаток уксусной кислоты.
В организме ацетилирующим реагентом является ацетилкофермент А - ключевой метаболит всех видов обмена в клетке.

г) образование амидов:
 | |||
 | |||
 + NH3 + HCl
+ NH3 + HCl
(амид уксусной
кислоты)
 | |||
 | |||

 O t° С
O t° С


 + NH3 CH3 – C + H2O
+ NH3 CH3 – C + H2O
 ONH4
ONH4
Амиды можно получить взаимодействием карбоновых кислот с аммиаком. Вначале образуются аммонийные соли, которые при нагревании теряют воду и превращаются в амиды. Амиды кислот подвержены различным превращениям. При нагревании с Р2О5 отщепляется вода и образуются нитрилы кислот:
 __
__
½ ½ t°, P2O5
 ½ ½ CH3–C=N + H2O
½ ½ CH3–C=N + H2O
½ ½ нитрил
½½ уксусной
кислоты
Все функциональные производные способны гидролизоваться с образованием карбоновых кислот:
 |  | ||
 + Н2О + НХ
+ Н2О + НХ

 ___
___

 ______ ½ ½
______ ½ ½
½ H½OH ½ ½

 R-C=½ N + H½OH ___
R-C=½ N + H½OH ___
½ H½OH -NH3 -H2O
При образовании функциональных производных карбоновых кислот мы сталкиваемся с двумя видами кислотных радикалов:
 | |||
 | |||
Ацил ацилат
 ----------------------------------------------------------------------------------------------
----------------------------------------------------------------------------------------------
 |
формил формиат
 | |||
 | |||
ацетил ацетат
 | |||
 | |||
пропионил пропионат
 | |||
 | |||
бензоил бензоат
Названия функциональных производных строятся по названию кислотных радикалов.
3. Реакции с участием радикалов монокарбоновых кислот. Углеводородные радикалы в карбоновых кислотах проявляют типичные химические свойства, соответствующие их природе: замещение – в насыщенных и ароматических углеводородных остатках кислот; присоединение, окисление, полимеризация – в ненасыщенных. При этом указанные реакции имеют некоторые особенности, обусловленные наличием карбоксильной группы:
а) галогенирование насыщенных алифатических кислот:
a t°
 СН3–СH2–СH–СООН + Br2 CH3 – CH2 – CH – COOH + HBr
СН3–СH2–СH–СООН + Br2 CH3 – CH2 – CH – COOH + HBr
½ ½
H Br
Замещение под действием галогенов идет избирательно у a - углеродного атома. Это объясняется появлением СН – кислотного центра у a - атома углерода под действием – I эффекта карбоксильной группы. Реакция используется для получения гетерофункциональных кислот - a-окси и a-аминокислот;
б) реакции присоединения к ненасыщенным кислотам: если в ненасыщенных кислотах карбоксильная группа вступает во взаимодействие с двойной связью, образуя систему сопряжения, то благодаря –М эффекту СООН – группы вся p-система смещена в сторону СООН – группы, что приводит к нарушению правила Марковникова в реакциях присоединения по двойной связи в углеводородном радикале:
d+  d-
d-
 СH2==CH ®COOH + HBr CH2 – CH – COOH
СH2==CH ®COOH + HBr CH2 – CH – COOH
½ ½
Br H
в) реакции окисления и полимеризации ненасыщенных кислот: эти реакции
протекают аналогично тем же реакциям алкенов:
KMnO4, H2O
 СН2 = СН – СООН СН2 – СН - СООН
СН2 = СН – СООН СН2 – СН - СООН
½ ½
ОН ОН
пропеновая 2,3 –дигидроксипропановая
 (акриловая)
(акриловая)


метиловый эфир метакриловой полиметилметакрилат
кислоты (плексиглас, органическое стекло)
г) реакции электрофильного замещения в ароматических кислотах:
 Карбоксильная группа за счет (–М) и (–I) - эффектов смещает электронную плотность бензольного кольца и направляет вновь поступающие электрофильные группы преимущественно в мета-положение. Например:
Карбоксильная группа за счет (–М) и (–I) - эффектов смещает электронную плотность бензольного кольца и направляет вновь поступающие электрофильные группы преимущественно в мета-положение. Например:
 |
t0
 d- + HO – NO2 + Н2О
d- + HO – NO2 + Н2О
3–нитробензойная кислота
|
Просмотров 1953 |
|
|
