
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Основные особенности геометрической изомерии
|
|
1. Существует только у соединений с двойными связями, при наличии заместителей у ненасыщенных атомов.
2. Транс-форма более симметрична, имеет более равномерное распределение электронной плотности. При симметричном строении дипольный момент транс-изомера равен 0.
3. Транс-форма обладает боле высокой температурой плавления вследствие большей симметричности кристаллов.
4. Транс-форма менее полярна, поэтому менее реакционноспособна и более устойчива.
5. Растворимость в воде больше у цис-формы, т.к. она более полярна.
ЛЕКЦИЯ 13
НИТРОПАРАФИНЫ
Определение
Это производные предельных углеводородов, у которых один или несколько атомов водорода замещено на группу NO2-нитрогруппу.
Классификация
1. По положению нитрогруппы подразделяются
| первичные | вторичные | Третичные |
| R-CH2-NO2 | R CH-NO2 R | R R-C-NO2 R |
2. По количеству нитрогрупп
а) мононитросоединения (с одной группой);
б) полинитросоединения (с двумя и более группами).
Изомерия
| CH3-NO2 CH3-CH2-NO2 | Нитрометан нитроэтан | Изомеров не имеют |
| CH3-CH2-CH2-NO2 NO2 CH3-CH-CH3 | 1-нитропропан 2-нитропропан | Изомеры положения |
| CH3-CH2-CH2-CH2-NO2 CH3 CH3-CH2-CH-NO2 CH3 CH3-C-NO2 CH3 | 1-нитробутан 2-нитробутан 2-нитро-2-метилпропан | Изомеры строения цепи |
Номенклатура
1. Рациональная – основа – нитрометан
2. Систематическая – основа – самая длинная цепь. Нумерация со стороны нитрогруппы.
CH3-CH-CH-CH3
NO2 CH3
Метилизопропилнитрометан (рациональная)
2-нитро-3-метилбутан (систематическая)
Получение
1. Нитрование парафинов по Коновалову (см. свойства предельных углеводородов)
2. Парофазное нитрование предельных углеводородов 67% HNO3 при 500-6000С.
3. Нитрование окисями азота
R + N2O4  RNO2 + NO2
RNO2 + NO2
4. Действие солей азотистой кислоты на галогенопроизводные (реакция Мейера-Коренблюме), может протекать в двух направлениях
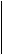
 C2H5-NO2 + NaBr
C2H5-NO2 + NaBr
C2H5Br + NaNO2- Нитроэтан
 C2H5-O-N=O + NaBr
C2H5-O-N=O + NaBr
Этилнитрит
Механизм – нуклеофильное замещение. Реагент – нитрит-анион, образующийся при диссоциации нитрита в результате сопряжения. Может давать две граничные структуры (с 1 и 2)
Na-O-N=O  Na+ + -O-N=O
Na+ + -O-N=O  O=N-O-
O=N-O-
Нитританион
Тогда равновесную структуру можно обозначить следующим образом
O-N-O
и назвать резонансной структурой.
Отрицательный заряд распределен поровну между атомами кислорода, а азот имеет неподеленную пару электронов. Взаимодействие нитританиона с галоидным алкилом может идти как за счет атома кислорода, так и азота. Если реакция идет по механизму SN1, то нитританион присоединяется по месту наибольшей электронной плотности, т.е. по кислороду, и образуется эфир.
CH3 CH3 CH3
CH-I  I- + +CH
I- + +CH  CH-O-N=O
CH-O-N=O
CH3 CH3 O—N=O CH3
Изопропилнитрит
Этому механизму способствует:
1. Использование третичных и вторичных галоидных алкилов;
2. Применение полярных растворителей (вода, спирт);
3. Использование AgNO2.
Если реакция идет по механизму SN2, то нитроанион присоединяется по месту наибольшей нуклеофильности (наибольшего сродства к углероду), т.е. по азоту, имеющему неподеленную пару электронов.
H CH3
 -
-  + O H CH3 O
+ O H CH3 O
Br  C + :N
C + :N  Br…C…N
Br…C…N  Br- + CH3-CH2-NO2
Br- + CH3-CH2-NO2
H O H O
Бромистый этил переходное состояние нитроэтан
Образуется нитросоединение.
Механизму SN2 способствует:
1. Использование первичных галоидных алкилов;
2. Апротонных растворителей;
3. Использование NaNO2.
|
Просмотров 714 |
|
|
