
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Ароматические альдегиды и кетоны
|
|
Ароматические альдегиды
1) Чисто ароматические

бензальдегид

о-, м-, п-толуиловый альдегид

2,4,5-триметилбензальдегид
2) жирноароматические

фенилуксусный альдегид

 -фенилпропионовый альдегид
-фенилпропионовый альдегид

 -фенилпропионовый альдегид
-фенилпропионовый альдегид
Ароматические кетоны
1) чисто ароматические

дифенилкетон (бензофенон)
2) жирноароматические
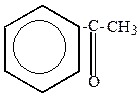
ацетофенон (метилфенилкетон)
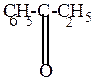
этилфенилкетон
Способы получения
I. Общие
1) окисление ароматических углеводородов с боковыми цепями
V2O5
C6H5CH3 + O2  H2O +
3000 H2O +
3000
| 
|
| толуол | бензальдегид |
2 степень окисления спирта
2) окисление спиртов
C6H5-CH2OH + O 
| 
| + H2O |
| бензиловый спирт | бензальдегид |
Окислители: MnO2 + H2SO4 + CuSO4
3) гидролиз дигалогенопроизводных
1000C
C6H5-CCl2-CH3 + H2O  2 HCl +
Fe 2 HCl +
Fe
| 
|
| метилфенилдихлорметан | ацетофенол (метилфенилкетон) |
5) сухая перегонка кальциевых солей карбоновых кислот
  CaCO3 + CaCO3 +
| 
|
| бензоат кальция | бензофенон (дифенилкетон) |
II. Частные способы получения альдегидов и кетонов
1) Реакция Фриделя-Крафтса

| + | 
| AlCl3 безв.
 -HCl
-HCl
| 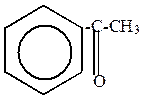
|
| хлористый ацетил (хлорангидрид уксусной кислоты) | ацетофенон |
Механизм – электрофильное замещение в ароматическом ядре.
2) Реакция Гаттермана – получение чисто ароматических альдегидов путем конденсации ароматических углеводородов с С=О.

|
 +
+ C=O +
+ C=O
|
+HCl
 (+AlCl3)
(+AlCl3)
| 
|
| толуол | п-толуиловый альдегид |
Механизм:
C=O + HCl 
| 
|
| хлористый формил |
Далее как в реакции Фриделя-Крафтса.
| CH3-C6H4-H + | 
| AlCl3
 -HCl
-HCl
| 
|
| толуол |
3) Реакция Тимана-Реймера
Конденсация фенолов с хлороформом в присутствии щелочей

| + | 
|
+ 3KOH
 -3 KCl
-H2O
-3 KCl
-H2O
| 
|
-H2O

| 
|
| салициловый альдегид |
Физические свойства
Ароматические альдегиды и кетоны – маслянистые жидкости или твердые вещества желтоватого цвета с приятным запахом.
Бензальдегид – миндаль, ацетофенол – черемуха. Мало растворимы в воде.
Химические свойства
Дают многие общие реакции альдегидов и кетонов.
1. Реакции нуклеофильного присоединения и замещения.
Активность ароматических карбонильных соединений в этих реакциях ниже активности карбонильных соединений жирного ряда, особенно низкой активностью обладают чисто ароматические кетоны.

| > | 
| > | 
| > | 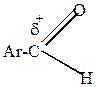
| > | 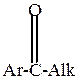
| > |
| > | 
|
Объясняется это следующим. Все углеводородные радикалы обладают электронодонорными свойствами и уменьшают +  у карбонильного углерода, снижая его способность к восприятию атаки нуклеофильного реагента. В ароматических карбонильных соединениях
у карбонильного углерода, снижая его способность к восприятию атаки нуклеофильного реагента. В ароматических карбонильных соединениях  -электронные связи С=О находятся в сопряжении с
-электронные связи С=О находятся в сопряжении с  -электронами ядра, происходит более значительное уменьшение +
-электронами ядра, происходит более значительное уменьшение +  карбонильного углерода, особенно у чисто ароматических кетонов.
карбонильного углерода, особенно у чисто ароматических кетонов.

Ароматические альдегиды не дают реакций полимеризации, чисто ароматические кетоны не присоединяют NaHSO3, не присоединяют Mg-органические соединения, не вступают в реакции конденсации друг с другом.
Ароматические альдегиды и кетоны могут присоединять HCN, образовывать оксимы, гидразоны, фенилгидразоны и т.д.

|
+ HCN 
| 
| |||
| циангидрин бензальдегида | |||||

|
+ H2N-OH  H2O + H2O +
| 
| |||
| ацетофенон | гидроксиламин | оксим ацетофенола | |||
2. Перегруппировка Бекмана
Наблюдается при действии на оксимы минеральных кислот.

|
+H+ 
|  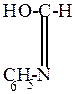
|

| 
|
| синбензальдоксим | ||||

| ||||
| N-фенилформамид |

|

| 
|

| 
|
| антибензальдоксим | бензамид |
Перегруппировка Бекмана заключается в том, что к радикалу или Н, находящимся в транс-положении к группе ОН, присоединяется к азоту со стороны неподеленной пары, а ее место занимает группа ОН.
Продуктами, образующимися в результате перегруппировки Бекмана, являются замещенные амиды (син- и анти-изомеры образуют различные амиды).
II. Реакции конденсации.
Чисто ароматические не способны к реакциям альдольной конденсации между собой, но для них характерны особые виды реакций конденсации.
1) реакция Канниццаро (самоокисления-самовосстановления)

| + | 
| t
+ KOH  C6H5-CH2OH +
конц. C6H5-CH2OH +
конц.
| 
| |
| бензальдегид | бензиловый спирт | калиевая соль бензойной кислоты | |||

| + | 
|
+ KOH  C6H5CH2OH + HCOOK C6H5CH2OH + HCOOK
| ||
Механизм:

| |||||

|
+ OH- 
| 
|

| 
|
 OH- + OH- +
|

| KOH
 омыление
омыление
|
Омыление
2) Бензоиновая конденсация

| + | 
| (KCN)

| 
|
| бензоин |
Механизм:

| ||||||

|
+ HCN- 
| 
| -H+

| 
|

| 
|
| протонная изомеризация | ||||||
 HCN + HCN +
| 
|
3) ароматические альдегиды и кетоны легко вступают в реакции конденсации с карбонилсодержащими соединениями жирного ряда, которые содержат подвижные атомы водорода в  -положении к карбонильной группе.
-положении к карбонильной группе.
а) реакция Перкина – реакция с ангидридами и сложными эфирами кислот

| + | 
| (СH3COONa)
 H2O + H2O +
| 
|

|
| бензальдегид | уксусный ангидрид | смешанный ангидрид коричной и уксусной кислоты | |||

| + CH3COOH | ||||
| коричная кислота |

| + | 
| (Na или C2H5ONa)
 H2O + H2O +
| 
|
| этилацетат | этиловый эфир коричной кислоты |
4) Реакция Клайзена – конденсация с альдегидами и кетонами жирного ряда

| |||||||

| + | 
|
 -H2O
-H2O
| 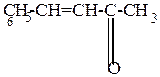
|
 -H2O
-H2O
| 
| |
| бензальдегид | бензальацетон | дибензальацетон | |||||
III. Реакции окисления и восстановления
1) Ароматические альдегиды чрезвычайно легко окисляются.
а) ароматические альдегиды окисляются кислородом воздуха – капля бензальдегида на часовом стекле через несколько минут закристаллизовывается.

| h  + O2
+ O2 
| 
|
Реакция идет по цепному перекисному механизму.

| h  + O2
+ O2  HOO. +
свет HOO. +
свет
| 
| ||||||||||||||||

|
+ O2 
| 
| ||||||||||||||||

| + | 
|

| 
| + | 
| ||||||||||||
| гидроперекись бензоила | ||||||||||||||||||

| + | 
|

| 
| ||||||||||||||
| гидроперекись бензоила | бензойная кислота | |||||||||||||||||
б) ароматические альдегиды легко окисляются слабыми окислителями, дают реакции серебряного зеркала с [Ag(NH3)4]OH

|
+ 2[Ag+(NH3)2]OH- 
| 
| +2Ag+3NH3+H2O |
2) Ароматические кетоны окисляются труднее, например, под действием сильных окислителей, при этом группа С=О всегда остается связанной с ароматическим ядром, например,

|
+3O  (KMnO4) (KMnO4)
| 
| + | 
|
| этилфенилкетон | бензойная кислота | уксусная кислота |
Хорошо протекает реакция окисления метилкетонов гипохлоритом.

|
+ 4 NaOCl  4 NaCl + 4 NaCl +
| 
| + H2O + CO2 |
| ацетофенон | гипохлорит натрия | бензойная кислота |
3) Восстановление карбоннльной группы может происходить под действием различных восстановителей атомарным или молекулярным водородом.
а) восстановление молекулярным водородом до спиртов.

| (Cu + Cr)
+ H2  C6H5-CH2OH C6H5-CH2OH
|
| бензальдегид | бензиловый спирт |
б) восстановление атомарным водородом до пинаконов

|
+ 2H  (Na в C2H5OH)
(Na в C2H5OH)
| 
|
| ацетофенон | 2,3-дифенол-2,3-бутиндиол |
в) восстановление до углеводородов происходит под действием амальгамированного цинка и кислоты.

|
+ 2 Zn(Hg) + 4 HCl  H2O + C6H5-CH2-CH3
(4H) H2O + C6H5-CH2-CH3
(4H)
|
| ацетофенон | этилбензол |
IV. Реакция замещения водорода.
а) легко замещается атом водорода в  -положении к группе С=О, например, жирноароматические кетоны галоидируются в присутствии железа.
-положении к группе С=О, например, жирноароматические кетоны галоидируются в присутствии железа.

|
+ Cl2  -HCl
-HCl
| 
|
| хлорметилфенилкетон (хлорацетофенон – ОВ со слезоточивым действием) |
б) Реакции электрофильного замещения протекают с малой скоростью в мета-положении к карбонильной группе –С-О
(группа С=О понижает электронную плотность ядра).
|
Просмотров 8944 |
|
|
