
Главная Обратная связь
Дисциплины:
Архитектура (936)
Биология (6393)
География (744)
История (25)
Компьютеры (1497)
Кулинария (2184)
Культура (3938)
Литература (5778)
Математика (5918)
Медицина (9278)
Механика (2776)
Образование (13883)
Политика (26404)
Правоведение (321)
Психология (56518)
Религия (1833)
Социология (23400)
Спорт (2350)
Строительство (17942)
Технология (5741)
Транспорт (14634)
Физика (1043)
Философия (440)
Финансы (17336)
Химия (4931)
Экология (6055)
Экономика (9200)
Электроника (7621)

Реакционноспособность некоторых заместителей в пиридиновом кольце
|
|
Особенностью соединений, содержащих пиридиновые кольца, является то, что некоторые заместители, введенные в различные положения к атому азота, проявляют различную реакционную способность.
1) Реакционноспособная группа ОН в оксипиридинах
а) оксигруппа в положении 3 (  ) – ведет себя как фенольная – взаимодействует с NaOH, FeCl3
) – ведет себя как фенольная – взаимодействует с NaOH, FeCl3
б) соединения с оксигруппой в положениях 2 или 4 (  или
или  ) существуют в таутомерном равновесии с кето-формой. Кислотные свойства их ниже и зависят от соотношения равновесных форм. Дают реакции спиртов и реакции кетоформы.
) существуют в таутомерном равновесии с кето-формой. Кислотные свойства их ниже и зависят от соотношения равновесных форм. Дают реакции спиртов и реакции кетоформы.

|
+ CH2N2 
| 
|



|
+ CH3I 
| 
|
2) Реакционноспособная группа NH2 в аминопиридине.
а) 3-аминопиридин по свойствам аналогичен ароматическим аминам: легко диазотируется, образуя соли диазония, которые распадаются с выделением азота и без выделения азота.

б) 2 и 4—аминопиридины существуют в таутомерных формах и дают реакции иминов.

|

| 
| H2O
 -NH3
-NH3
| |||

|

| 
| ||||
В обычных условиях не диазотируются, что объясняется малой устойчивостью диазокатиона.

3) реакционноспособность углеводородных радикалов при расположении радикала в  или
или  -положении очень сильно увеличивает подвижность атома Н в
-положении очень сильно увеличивает подвижность атома Н в  -положении к азоту.
-положении к азоту.
а) взаимодействие  и
и  -пиколинов с С4Н9Zn;
-пиколинов с С4Н9Zn;

|
+C4H9Li  C4H10 + C4H10 +
| 
|
б) взаимодействие  -пиколинов с бензальдегидом.
-пиколинов с бензальдегидом.

| + | 
| 2250
(ZnCl2)
 -H2O
-H2O
| 
|
4) Реакционноспособность атома галогена: в  -положении – пониженная (как у галогена, связанного с ароматическим ядром); в
-положении – пониженная (как у галогена, связанного с ароматическим ядром); в  и
и  -положениях – пониженная (как у соединений жирного ряда или как у ароматических с группой NO2 в о- и п-положениях). Легко замещается на NH2, OH, OR, CN и другие.
-положениях – пониженная (как у соединений жирного ряда или как у ароматических с группой NO2 в о- и п-положениях). Легко замещается на NH2, OH, OR, CN и другие.

| + | 
|

| 
|
Между собой такие молекулы могут образовывать соли с отщеплением иона галогена.
Конденсированные системы с шестичленными гетероциклами

| 
| 
|
| хинолин | изохинолин | акридин |
Окислением каптакса получают дисульфид – альтакс.
Получение
1) Реакция Скраупа – конденсация первичных ароматических аминов с глицерином в присутствии серной кислоты и окислителей.

|
+H2SO4
 -2H2O
-2H2O
| 
|

| 
| ||||||
| акролеин (непредельный альдегид) | ||||||||||

| + | 
|

| 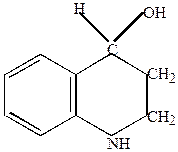
|
+O (C6H5NO2)
 -2H2O
-2H2O
| |||||

| 
| |||||||||
2) Реакция Битлера-Напиральского – действие фосфорного ангидрида на  -фенилалкиламиды кислот.
-фенилалкиламиды кислот.

| тауто
мери
зация

| 
| P2O5
 -H2O
-H2O
| 
|

|
 -фенил-N-этиламид уксусной кислоты -фенил-N-этиламид уксусной кислоты
| таутомерная форма | ||||
Pd
 -H2
-H2
| 
| ||||
| 1-метилизохинолин |
3) Конденсация  -фенилалкиламинов с формальдегидом.
-фенилалкиламинов с формальдегидом.

|
P2O5
 -H2O
-H2O
| 
|
Pd
 -2H2
-2H2
| 
|
 -фенилэтиламин -фенилэтиламин
| изохинолин |
4) Выделение из каменноугольной смолы.
Химические свойства конденсированных гетероциклов определяются: 1) наличием аминного азота, который придает соединению слабые основные свойства; 2) реакциями ароматического бензольного и гетероциклического ядер.
В хинолине реакции электрофильного замещения идут легче, чем у пиридина, но, в основном, в положениях 5 и 8, т.е. в  -положениях более активного в реакциях электрофильного замещения бензольного ядра.
-положениях более активного в реакциях электрофильного замещения бензольного ядра.

Реакции нуклеофильного замещения идут, как и у пиридина, в  - или
- или  положениях к азоту в пиридиновом кольце.
положениях к азоту в пиридиновом кольце.
В реакции окисления легче вступают гомологи (за счет окисления боковых цепочек).

| 3O
 -H2O
-H2O
| 
|
| хинальдин | хинальдиновая кислота (применяется в аналитической химии для обнаружения Cd, Cu, Zn, Fe). |
Незамещенные гетероциклы окисляются за счет разрушения бензольного ядра (пиридиновое ядро к окислению устойчивее).
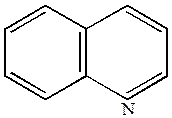
|
+ 9O  (KMnO4) (KMnO4)
| 
| + 2CO2 + H2O |
| 2,3-пиридиндикарбоновая кислота (хинолиновая) |
Восстановление идет за счет присоединения водорода к пиридиновому кольцу.
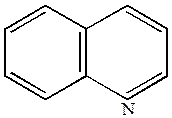
|
+ 4H  (C2H5OH + Na)
(C2H5OH + Na)
| 
|
| тетрагидрохинолин |
Гидрирование бензольного кольца протекает только в присутствии катализаторов. Из производных хинолина большое применение в аналитической химии имеет 8-оксихинолин (оксин).
Он способен образовывать с ионами металлов Mg, Ca, Cr и др. комплексные нерастворимые соли – хелаты (оксинаты).

|
+ MgCl2  2 NaCl + 2H2O +
2NaCl 2 NaCl + 2H2O +
2NaCl
| 
|
Все перечисленные соединения данной группы применяются для синтеза различных медицинских препаратов, для получения красителей. Многие их производные являются алкалоидами.
Понятие об алкалоидах
Алкалоиды – это широко распространенная группа природных органических оснований, преимущественно растительного происхождения, содержащих в молекуле какие-либо азотсодержащие гетероциклы и обладающие сильным физиологическим действием (обезболивающее, угнетающее, возбуждающее). Вследствие этого многие алкалоиды применяются как лекарственные вещества.
Название “алкалоиды” происходит от слова алкали - щелочь.
Примеры алкалоидов.
Алкалоиды группы пиридина
| Коннин – главный алкалоид болиголова | 
|  -пропилпиперидин (яд Сократа) -пропилпиперидин (яд Сократа)
|
| Никотин – главный алкалоид табака | 
|  , N-метилпирролидил- , N-метилпирролидил-  -пиридин -пиридин
|
Алкалоиды группы хинолина
Хинин

К алкалоидам относятся также кокаин, морфин (опий), теин (чай), салонин (главный алкалоид картофеля, содержится в зеленом чае), кодеин, атропин, пилокарпин и многие другие. Алкалоиды широко используются в медицине. Многие из них в больших дозах являются ядами. При частом и регулярном употреблении алкалоидов может произойти привыкание организма и появление болезненного состояния - наркомании.
|
Просмотров 910 |
|
|
